
下图是电解CuCl2溶液的装置,其中c、d为石墨电极,则以下有关此电解池的判断正确的是( )

A.a为负极、b为正极
B.a为阳极、b为阴极
C.电解过程中,d电极质量增加
D.电解过程中,氯离子浓度不变
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016届江苏省高三上学期第二次质检化学试卷(解析版) 题型:选择题
短周期主族元素X 、Y 、Z、W的原子序数依次增大,X原子核外最外层电子数是次外层的2倍,Y的氟化物YF3分子中各原子均达到8电子稳定结构,Z是同周期中原子半径最大的元素,W的最高正价为+7价.下列说法正确的是( )
A.简单离子半径大小顺序:rW>rZ>rY
B.元素W的氧化物对应水化物的酸性比Y 的强
C.X与Y形成的原子晶体X3Y4的熔点可能比金刚石高
D.X与W形成的化合物和Z与W形成的化合物的化学键类型相同
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省济宁任城区高二上学期统考化学试卷(解析版) 题型:选择题
已知反应:(NH4)2CO3(s)=NH4HCO3(s)+NH3(g) △H=+74.9kJ.mol-1,下列说法中正确的是
A.该反应中熵变、焓变皆大于0
B.该反应是吸热反应,因此一定不能自发进行
C.在碳酸盐分解反应中熵增加,因此任何条件下所有碳酸盐的分解一定能自发进行
D.能自发进行的反应一定是放热反应,不能自发进行的反应一定是吸热反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省雅安市高一上学期12月月考化学试卷(解析版) 题型:选择题
除去粗盐溶液中的Ca2+、Mg2+、SO42-等杂质,需依次加入稍过量的NaOH溶液、X溶液、Y溶液,过滤,最后向滤液中滴加稀盐酸调至中性。其中X、Y分别是
A.Na2CO3 Ba(NO3)2 B. Na2CO3 AgNO3
C. Na2CO3 BaCl2 D. BaCl2 Na2CO3
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高二上学情调查化学试卷(解析版) 题型:选择题
下列叙述不正确的是
A.0.1 mol•L-1氨水中,c(OH-)>c(NH4+)
B.等体积等物质的量浓度的NaX和弱酸HX混合后的溶液中:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-)
C.在0.1 mol•L-1CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+)
D.0.1 mol•L-1某二元弱酸强碱盐Na2A溶液中,c(Na+)=2c(A2-)+2c(HA-)+2c(H2A)
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三上12月月考化学试卷(解析版) 题型:选择题
在密闭容器中充入一定量的NO2,发生反应2NO2(g) N2O4(g)
N2O4(g) 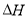 =-57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如下图所示。下列说法正确的是
=-57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如下图所示。下列说法正确的是
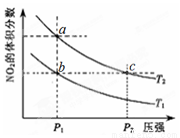
A.a、c两点的反应速率:a>c
B.a、b两点NO2的转化率:a<b
C.a、c两点气体的颜色:a深,c浅
D.由a点到b点,可以用加热的方法
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三上学期期末理综化学试卷(解析版) 题型:填空题
Ni元素化合物在生活中有非常重要的应用。纳米NiO可以制备超级电容器,NiOOH是制作二次电池的重要材料。现以NiSO4为原料生产纳米NiO和NiOOH流程如下:
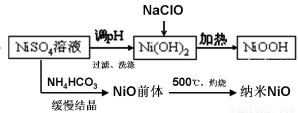
(1)制备NiOOH过程中,NiSO4溶液配制方法__________________;过滤、洗涤后,得到Ni(OH)2固体,如何证明Ni(OH)2已经完全洗净______________;NaClO氧化Ni(OH)2的离子方程式为_________________。
(2) 已知Ksp[Ni(OH)2] = 2×10-15。室温下,欲加入一定量 NaOH固体使1L 含有0.001 mol·L-1的NiSO4和0.0001 mol·L-1的H2SO4溶液中残留c(Ni2+)≤2×10-7 mol·L-1,并恢复至室温,所加入的NaOH的固体质量至少为________g。
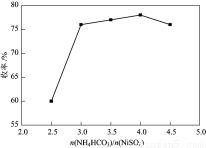
(3)NH3·H2O的浓度对纳米NiO的产率产生很大影响。右图为NiSO4的物质的量一定时,不同的反应物配比对纳米氧化镍收率的影响。请解释反应物NH4HCO3 和NiSO4 的物质的量比在2.5至4.0时,收率升高的原因__________________。
(4)制备纳米 NiO 时,加入一些可溶于水的有机物(如:吐温—80)能制得更优质的纳米材料,原因是__________________。
(5)沉降体积是超细粉体的一个重要参数,若颗粒在液相中分散性好,则沉降体积较小;若颗粒分散性较差,则易引起絮凝沉降体积较大。右图是吐温—80 的加入量与前体在液体石蜡中沉降体积的关系曲线。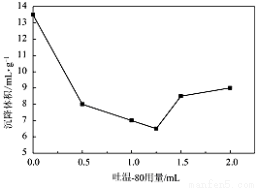
通过右图分析,吐温—80的最佳加入量为__________mL。
(6)NiOOH是制备镍镉电池的原料,某镍镉电池的总反应为
Cd+2NiOOH + 2H2O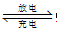 Cd(OH)2+ 2Ni(OH)2
Cd(OH)2+ 2Ni(OH)2
该电池放电时正极电极反应式为______________________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上12月月考化学试卷(解析版) 题型:选择题
有关如下图所示原电池(盐桥中装有含琼胶的KCl饱和溶液)的叙述,正确的是
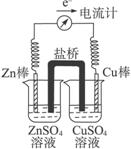
A.铜棒上有气泡逸出
B.取出盐桥后,电流计依然发生偏转
C.反应中,盐桥中的K+会移向CuSO4溶液
D.反应前后铜棒质量不改变
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一上学期12月月考化学试卷(解析版) 题型:选择题
用氢氧化钠固体配制0.10 mol/L的氢氧化钠溶液,下列说法中不正确的是
A.定容时俯视容量瓶刻度线,会造成所配溶液浓度偏大
B.定容摇匀后发现液面下降,不应再加蒸馏水
C.称量时托盘上要垫上干净的称量纸
D.移液时不慎有部分液体溅出,会造成所配溶液浓度偏小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com