
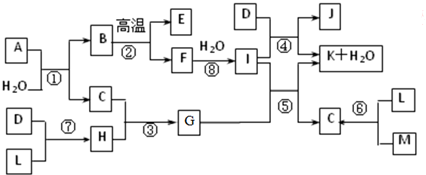
分析 图中各物质是由1~20号元素中部分元素组成的单质或其化合物,D、L、M为气体单质,可能为H2、O2、N2、Cl2中的一种,C、E、H为气体化合物,L、M反应生成C,且是化工生产中的重要反应,D、L反应生成H,反应⑤是实验室制备气体C的重要方法,则可推断C为NH3,L为H2,D为Cl2,M为N2,则G为NH4Cl,根据题中各物质转化关系结合反应④是化工生产中的重要反应,可进一步推得I为Ca(OH)2,K为CaCl2,J为Ca(ClO)2,反应④应是工业制备漂白粉原理,可以反应推得F为CaO,反应②是化工生产中的重要反应,为碳酸钙高温分解反应,故B为CaCO3、E为CO2.物质A由三种元素组成,1molA与水反应可生成1molB(CaCO3)和2molC(NH3),根据元素守恒可知A含有Ca、C、N三种元素,由原子守恒可知,A的化学式为CaCN2,据此解答.
解答 解:图中各物质是由1~20号元素中部分元素组成的单质或其化合物,D、L、M为气体单质,可能为H2、O2、N2、Cl2中的一种,C、E、H为气体化合物,L、M反应生成C,且是化工生产中的重要反应,D、L反应生成H,反应⑤是实验室制备气体C的重要方法,则可推断C为NH3,L为H2,D为Cl2,M为N2,则G为NH4Cl,根据题中各物质转化关系结合反应④是化工生产中的重要反应,可进一步推得I为Ca(OH)2,K为CaCl2,J为Ca(ClO)2,反应④应是工业制备漂白粉原理,可以反应推得F为CaO,反应②是化工生产中的重要反应,为碳酸钙高温分解反应,故B为CaCO3、E为CO2.物质A由三种元素组成,1molA与水反应可生成1molB(CaCO3)和2molC(NH3),根据元素守恒可知A含有Ca、C、N三种元素,由原子守恒可知,A的化学式为CaCN2.
(1)E为CO2,其结构式为O=C=O,故答案为:O=C=O;
(2)属于化合反应,但不属于氧化还原反应的是③⑧,故答案为:③⑧;
(3)由上述分析可知,A的化学式为CaCN2,故答案为:CaCN2;
(4)反应④的离子反应方程式为:Cl2+Ca(OH)2=Ca2++Cl-+ClO-+H2O,
故答案为:Cl2+Ca(OH)2=Ca2++Cl-+ClO-+H2O;
(5)检验集气瓶中气体是否为Cl2的操作方法是:将湿润的淀粉KI试纸贴在玻璃棒上,伸入集气瓶,试纸变蓝证明为氯气,
故答案为:将湿润的淀粉KI试纸贴在玻璃棒上,伸入集气瓶,试纸变蓝证明为氯气.
点评 本题考查无机物的推断,基本属于猜测验证型题目,根据物质的状态和类别,结合中学常见的重要化工反应进行推断,侧重学生对元素化合物知识的熟练掌握考查,难度较大,综合性强.


科目:高中化学 来源: 题型:实验题
| 实验操作 | 实验现象 |
| ①取10ml一定溶质质量分数的硫酸铜溶液,倒入50ml的烧杯里 ②取一块钠,用滤纸吸干表面煤油,再切取绿豆大小的一块,投入溶液中 | 钠浮在液面上,熔化成闪亮小球,钠球游动,发出“嘶嘶”的声响,析出蓝色沉淀 |
| 实验操作 | 实验现象 | 结论 |
| 取烧杯中少许沉淀于试管中,再向其中加入过量的稀硫酸 | 沉淀全部溶解,溶液变蓝色 | 说明沉淀中不含红色的铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | CO的含量保持不变 | |
| B. | 容器中CH3OCH3浓度与CO2浓度可能相同 | |
| C. | 3V正(CO)=V正(CH3OCH3) | |
| D. | 体系的温度保持不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 因为SiO2能与强碱溶液反应,所以盛装强碱溶液的试剂瓶不用玻璃塞 | |
| B. | 因为SO2可以使溴水褪色,所以SO2具有漂白性 | |
| C. | 因为某碱性溶液的焰色呈黄色,所以其溶质为NaOH | |
| D. | 因为NH3的水溶液可以导电,所以NH3是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,B的结构式为
,B的结构式为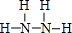 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气态氢化物的稳定性:X>Y | |
| B. | Y和M元素的最高正价相同 | |
| C. | X、Z分别与Y形成的化合物中,化学键类型相同 | |
| D. | Z的最高氧化物的水化物是强碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同条件下,溶液中Fe3+、Cu2+、Zn2+的氧化性依次减弱 | |
| B. | 常温常压下,足量的Fe在1 mol Cl2中充分燃烧,转移的电子数为2NA(NA为阿伏加德罗常数的值) | |
| C. | 卤族元素单质X2(X:代表F、Cl、Br、I)均可以与水反应生成HXO | |
| D. | SiO2既能和氢氧化钠溶液反应也能和氢氟酸反应,所以是两性氧化物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com