
下列金属不能在氧气中剧烈燃烧的是( )
A.Mg B.Al
C.Fe D.Cu
科目:高中化学 来源: 题型:
某稀溶液中含有等物质的量的ZnSO4, Fe2(SO4)3, H2 SO4, CuSO4,向其中逐渐加入铁粉,溶液中Fe2+的物质的量(纵坐标/mol)和加入铁粉的物质的量(横坐标/mol)之间的关系为( )
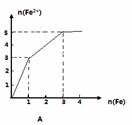
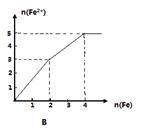

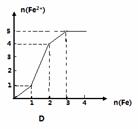
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中含有的溶质是FeBr2、FeI2,若先向该溶液中通入一定量的氯气,再向反应后的溶液中滴加KSCN溶液,结果溶液变为红色,则下列叙述正确的是
A.原溶液中的Br-一定被氧化B.通入氯气之后原溶液中的Fe2+不一定被氧化
C.不能确定通入氯气之后的溶液中是否存在Fe2+
D.若取少量所得溶液,再加入CCl4溶液,静置、分液,向上层溶液中加入足量的AgNO3 溶液,能产生黄色沉淀。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应:4NH3(g)+5O2(g) = 4NO(g)+6H2O(g),若化学反应速率分别是用v(NH3)、v(O2)、v(NO)、v(H2O) [单位均为mol·L-1·S-1]
A.4/5 v(NH3)= v(O2) B.5/6 v(O2)= v(H2O)
C.2/3 v(NH3)= v(H2O) D.4/5 v(O2)= v(NO)
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,在一个2 L的密闭容器中,加入4 mol A和2 mol B 进行如下反应:3A(g)+2B(g)  4C(s)+2D(g),反应一段时间后达到平衡,测得生成
4C(s)+2D(g),反应一段时间后达到平衡,测得生成
1.6 mol C,则下列说法正确的是
A.该反应的化学平衡常数表达式是K=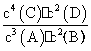 B.此时,B的转化率是40%
B.此时,B的转化率是40%
C.增大该体系的压强,平衡向右移动,化学平衡常数增大
D.增加B,平衡向右移动,B的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是某种常见金属的部分性质:
| 颜色状态 | 硬度 | 密度 | 熔点 | 导电性 | 导热性 | 延展性 |
| 银白色固体 | 较软 | 2.70 g·cm-3 | 660.4℃ | 良好 | 良好 | 良好 |
将该金属投入冷水中无变化,投入稀盐酸中可产生大量的无色气体。试回答:
(1)推断该金属可能的一种用途:________,该金属的活泼性比铜________(填“强”或“弱”)。
(2)请自选试剂,设计不同的实验方案探究该金属与铁的活泼性强弱,并完成下表:
| 猜想 | 验证方法 | 预测实验现象 |
| 该金属比铁活泼 | ||
| 该金属活泼性比铁弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列与化学反应能量变化相关的叙述正确的是
A.生成物总能量一定低于反应物总能量
B.应用盖斯定律,可计算某些难以直接测量的反应焓变
C.人类利用的能量都是通过化学反应获得的
D.在化学反应中只有燃烧反应才能放出热量
查看答案和解析>>
科目:高中化学 来源: 题型:
以电解食盐水为基础制取氯气等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一。
(1)电解饱和食盐水的化学方程 式为 ▲ 。
式为 ▲ 。
 (2)常温下,某化学兴趣小组在实验室中,用石墨电极以右图装置进行电解某浓度氯化钠溶液的实验,电解一段时间后,收集到标准状况下氢气2.24L。(设电解前后溶液的体积均为1 L,不考虑水的消耗或气体的溶解)
(2)常温下,某化学兴趣小组在实验室中,用石墨电极以右图装置进行电解某浓度氯化钠溶液的实验,电解一段时间后,收集到标准状况下氢气2.24L。(设电解前后溶液的体积均为1 L,不考虑水的消耗或气体的溶解)
①理论上,电解后溶液中c(OH—)= ▲ mol/L。
②若实际测得反应后溶液的c(OH—)=0.1mol/L,则造成这种误差的原因可能是:
a.2H2O 2H2↑+O2↑;若仅考虑该原因,则电解过程中溶液减小的质量是 ▲ g。
2H2↑+O2↑;若仅考虑该原因,则电解过程中溶液减小的质量是 ▲ g。
b.还可能为 ▲ (用离子方程式表示)。
③经测定,该实验中溶液实际减少的质量为4.23g,则所产生的气体及其物质的量之比为
▲ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com