
写出下列物质的化学式,并进行物质的分类(按单质、酸性氧化物、碱性氧化物、酸、碱、正盐、酸式盐、碱式盐)。
(1)磷酸 、 ; (2)纯碱 、 ;
(3)铜绿 、 ; (4)小苏打 、 ;
(5)硝酸亚铁 、 ; (6)氩 、 。
(1)H3PO4、酸;(2)Na2CO3,盐;(3)Cu2(OH)2CO3,碱式盐;(4)NaHCO3、酸式盐;(5)Fe(NO3)2、盐;(6)Ar、单质。
本题是对常见物质名称、化学式及常见分类方法的考查。H3PO4电离出的阳离子只有H+,属于酸;纯碱、铜绿、NaHCO3、Fe(NO3)2均可电离出金属阳离子和酸根阴离子,属于盐;但NaHCO3中的HCO3-还可继续电离出一个H+,属于酸式盐;铜绿的化学式为Cu2(OH)2CO3,属于碱式盐。
值得一提的是:分类法是一种行之有效、简单易行的科学方法。根据不同需要,按不同标准,可以有多种分类方法。同学们可以尝试从颜色、状态、溶解性几个角度对其进行分类。


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
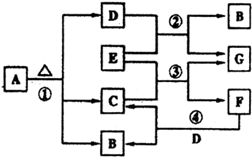 已知固体A的焰色反应呈黄色,D、G常温下呈气态,化合物E为淡黄色固体粉末,A、B、C、D、E、F、G有如图转化关系:
已知固体A的焰色反应呈黄色,D、G常温下呈气态,化合物E为淡黄色固体粉末,A、B、C、D、E、F、G有如图转化关系:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
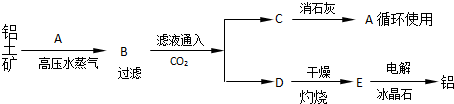
| Al2O3 | Fe2O3 | Na2O | |
| 铝土矿 | 55% | 16% | 0% |
| 赤泥 | 15% | 48% | 8% |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com