
| A. | SiO2和CO2中,Si和O、C和O之间都是共价键 | |
| B. | 离子化合物中一定有金属元素 | |
| C. | 蛋白质溶液、淀粉溶液和蔗糖溶液都是胶体 | |
| D. | 共价化合物中各原子都满足8电子稳定结构 |
分析 A.非金属元素之间以共用电子对形成化学键;
B、离子化合物氯化铵都是非金属元素;
C、蔗糖溶液不是胶体;
D、由氢形成的氢化物中氢只是2电子的稳定结构.
解答 解:A.非金属元素之间以共用电子对形成化学键,则SiO2和CO2中Si和O,C和O之间都是共价键,故A正确;
B、离子化合物氯化铵都是非金属元素,不一定存在金属元素,故B错误;
C、蔗糖溶液不是胶体,故C错误;
D、由氢形成的氢化物中氢只是2电子的稳定结构,如水中的氢是2个电子的稳定结构,故D错误;
故选A.
点评 本题为综合题,为高考中常见的冷拼凑试题,涉及共价键、离子化合物的组成、胶体、电子式等,侧重物质性质的考查,具有坚实的基础知识即可解答,题目难度不大.


科目:高中化学 来源: 题型:解答题

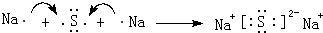 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca2+、Cl-、$MnO_4^-$、Na+ | B. | K+、Cl-、$SO_4^{2-}$、H+ | ||
| C. | OH-、Na+、Al3+、I- | D. | H+、Cl-、Ba2+、Ag+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 现有反应:A、CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
现有反应:A、CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ 查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钚是f 区元素 | B. | 核外电子数238 | C. | 核内中子数 144 | D. | 钚是锕系元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸铝溶液中加入过量的氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| B. | 氯化镁溶液中加入氢氧化钠溶液:Mg2++2OH-═Mg(OH)2↓ | |
| C. | 大理石溶于醋酸中:CaCO3+2CH3COOH═Ca2++2CH3COO-+CO2↑+H2O | |
| D. | NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-═CO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | W元素是硅元素 | |
| B. | 气态氢化物的稳定性:Y<R | |
| C. | X、W、Y的最高价氧化物的水化物酸性强弱顺序是X<Y<W | |
| D. | X、Y、W、R的原子半径由大到小的顺序为R>W>X>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 原子半径大小为:B>A>C | B. | 核电荷数:D>C>B>A | ||
| C. | A与D形成的化合物均是离子键 | D. | 生成的氢化物的稳定性为:D>A>B |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com