
向密闭容器中充入物质A和B,发生反应aA(g)+bB(g)  cC(g)。反应过程中,物质A的体积分数和C的体积分数随温度(T)的变化曲线如图所示,下列说法正确的是( )
cC(g)。反应过程中,物质A的体积分数和C的体积分数随温度(T)的变化曲线如图所示,下列说法正确的是( )

A.该反应在T1、T3温度时达到化学平衡
B.该反应在T2温度时达到化学平衡
C.该反应的逆反应是放热反应
D.升高温度,平衡会向正反应方向移动
科目:高中化学 来源:2016届贵州省高三5月高考模拟理综化学试卷(解析版) 题型:选择题
电解NO制备NH4NO3,其工作原理如图所示,下列说法不正确的是( )
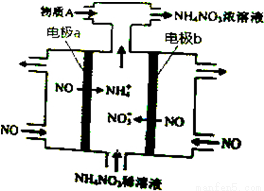
A.b极的电极反应为:NO-3e-+2H2O=NO3-+4H+
B.溶液中的H+由电极a处向电极b处迁移
C.电解过程总反应的化学方程式为:8NO+7H2O 3NH4NO3+2HNO3
3NH4NO3+2HNO3
D.为使电解产物全部转化为NH4NO3,需补充的物质A是NH3
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省汕头市高二下期末化学试卷(解析版) 题型:选择题
下列关于有机物的说法中,不正确的是
A.用水能够鉴别苯和溴苯
B.苯不能使KMnO4溶液褪色,因此苯不能发生氧化反应
C.除去乙醇中少量的乙酸:加入足量生石灰,蒸馏
D.氯乙烯分子内所有原子均在同一平面
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二下期中化学试卷(解析版) 题型:实验题
水合肼 (N2H4·H2O) 常用作还原剂和抗氧剂,其熔点为 -40℃,沸点 118.5℃,极毒。实验室用如下装置制取水合肼(N2H4·H2O)涉及下列反应:
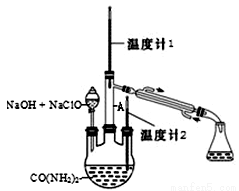
CO(NH2)2+ 2NaOH +NaClO = Na2CO3 + N2H4·H2O + NaCl
N2H4·H2O + 2NaClO = N2↑ + 3H2O + 2NaCl]
请回答下列问题:
(1)配制30%NaOH溶液时,所需玻璃仪器除量筒外,还有 (填标号)。
A.容量瓶 B.烧杯 C.烧瓶 D.玻璃棒
(2)将Cl2通入30%NaOH溶液制备NaClO的化学方程式 。
(3)实验时,如果将 NaOH 和NaClO的混合溶液一次性加入三颈烧瓶,可能会造成的结果是__________。
(4)实验时可根据_________判断N2H4·H2O开始蒸出。
(5)已知:N2H4·H2O + 2I2= N2↑+ 4HI + H2O。测定水合肼的质量分数可采用下列步骤:
①取1.250g试样,经溶解、转移、定容等步骤,配制250mL溶液。
②移取10.00mL溶液于锥形瓶中,滴入几滴淀粉溶液,加20mL水,摇匀。
③将0.1 000mol·L-1碘的标准溶液盛放在__________滴定管中(填“酸式”或“碱式”),当_____________停止滴定,消耗碘的标准溶液为18.00mL,则产品中N2H4·H2O的质量分数为__________。
000mol·L-1碘的标准溶液盛放在__________滴定管中(填“酸式”或“碱式”),当_____________停止滴定,消耗碘的标准溶液为18.00mL,则产品中N2H4·H2O的质量分数为__________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二下期中化学试卷(解析版) 题型:选择题
某无色混合气体可能由H2、O2、NH3、N2、CO2、HCl和He中的两种或多种组成。常温下取此气体200mL进行实验,实验的过程和结果如下(上述气体的体积都是折算成相同条件下的体积)。下列说法错误是
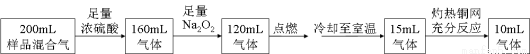
A.原混合气体中有5ml O2
B.原混合气体中肯定存在NH3,肯定不存在HCl
C.原混合气体中CO2的体积分数为40%
D.可能存在N2或He,它们在原混合气体中的体积分数不可能超过5%
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二下期中化学试卷(解析版) 题型:选择题
下列有关钢铁腐蚀和防护的说法不正确的是( )
A.自行车的钢圈上镀一层铬,防止生锈
B.外加直流电源保护钢闸门时,钢闸门与电源的负极相连
C.钢铁发生吸氧腐蚀的正极反应:2H2O+O2 - 4e-===4OH-
D.钢铁发生析氢腐蚀的负极反应:Fe-2e-===Fe2+
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二下期中化学试卷(解析版) 题型:选择题
化学是一门以实验为基础的自然科学,化学实验在化学学习中具有极其重要的作用。下列实验中所选用的仪器合理的是( )
①用50 mL量筒量取5.2 mL稀硫酸
②用分液漏斗分离苯和四氯化碳的混合物
③用托盘天平称量11.7 g氯化钠晶体
④用碱式滴定管量取23.10 mL溴水
⑤用瓷坩埚灼烧各种钠化合物
⑥用250 mL容量瓶配制250 mL 0.2 mol/L的NaOH溶液
A.①②④ B.②③④⑥ C .③⑥ D.③⑤⑥
.③⑥ D.③⑤⑥
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高一下期中化学试卷(解析版) 题型:推断题
随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。

根据判断出的元素回答问题:
(1)g在周期表中的位置是________。
(2)比较g、h的最高价氧化物对应水化物的酸性强弱:________>________。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式:________。
(4)已知1 mol e的单质在足量d2中燃烧,恢复至室温,放出255.5 kJ热量,写出该反应的热化学方程式:________。
(5)上述元素可组成盐R:zx4f(gd4)2。向盛有 10 mL 1 mol·L-1R溶液的烧杯中滴加1 mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积的变化示意图如下:
10 mL 1 mol·L-1R溶液的烧杯中滴加1 mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积的变化示意图如下:

①写出m点反应的离子方程式:________。
②若在R溶液中改加20 mL 1.2 mol·L-1Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为________mol。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高二下期中化学试卷(解析版) 题型:选择题
H2S是一种有臭鸡蛋气味的气体,其分子结构和H2O相似,但S—H键键能比O—H键键能低。下列判断错误的是( )
A.H2S分子呈V形
B.H2S沸点低于H2O沸点,因为S—H键键能低
C.H2S分子中只含σ键
D.H2S分子稳定性低于H2O分子,因为O—H键键能高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com