
某化学实验小组拟用50mLNaOH溶液吸收CO2气体(用大理石和稀盐酸反应来制取CO2),以制备纯净的Na2CO3溶液。为了防止通入的CO2气体过量生成NaHCO3,他们设计了如下实验过程:
a.取25 mL NaOH溶液,向其中通入过量的CO2气体,至CO2气体不再溶解;
b.小火煮沸此溶液1~2 min;
c.在得到的溶液中加入另一半(25mL)NaOH溶液,使其充分混合反应。
(1)此方案能制得较纯净的Na2CO3,写出a、c两步的化学反应方程式:____________________________________、_____________________________________
(2)煮沸溶液的目的是 。
此方案第一步的实验装置如右图所示: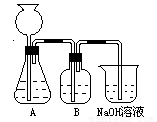
(3)加入反应物前,如何检查整个装置的气密性_________________________________。
(4)装置B中盛放的试剂是____________,作用是__________________________________。
(5)在实验室制法中,装置A还可作为下列_____________气体的发生装置(填序号)。
①CH2=CH2 ②H2S ③CH4 ④CH≡CH ⑤H2
(6)实验室制取下列气体:①NH3,②Cl2,③HCl,④H2S,⑤CH4,⑥CO,⑦CO2,⑧O2时,属于必须进行尾气处理并能用下图所示装置进行处理的,将气体的序号填入装置图的下方空格内。
尾 气 吸 收 装 置 |
|
|
处理气体 |
|
|
(7)已知所用NaOH溶液中溶质的质量分数为40%,室温下该溶液密度为1.44 g / mL,假设反应前后溶液的体积不变,不考虑实验误差,计算用此种方法制备所得Na2CO3溶液的物质的量浓度为_________________。
(1)NaOH+CO2=NaHCO3 NaHCO3+NaOH=Na2CO3+H2O;
(2)充分将溶液中多余的CO2赶走;
(3)将连接B和烧杯间的乳胶管用止水夹夹住。然后从漏斗注入一定量的水,使漏斗中的水面高于锥形瓶内的水面,过一会,观察漏斗内与锥形瓶中的液面差,若保持不变,说明装置不漏气;
(4)饱和NaHCO3溶液,吸收HCl气体;
(5)②⑤;(6)①③,②④;(7)7.2mol/L
【解析】
试题分析:(1)此方案能制得较纯净的Na2CO3, a、c两步的化学反应方程式是:NaOH+CO2=NaHCO3 NaHCO3+NaOH=Na2CO3+H2O;(2)由于CO2能够在水中溶解,所以煮沸溶液的目的是充分将溶液中多余的CO2赶走;(3)加入反应物前,检查整个装置的气密性的方法是将连接B和烧杯间的乳胶管用止水夹夹住。然后从漏斗注入一定量的水,使漏斗中的水面高于锥形瓶内的水面,过一会,观察漏斗内与锥形瓶中的液面差,若保持不变,说明装置不漏气;(4)装置B中盛放的试剂是饱和NaHCO3溶液,作用是吸收CO2气体中的杂质HCl气体;(5)装置A是固体与液体反应制取气体,反应不能加热,①CH2=CH2是乙醇与浓硫酸混合加热170 ℃时发生消去反应制取乙烯,不能使用该装置,错误;②H2S是FeS与稀HCl反应来制取,不用加热,制取;③CH4是无水乙酸钠和碱石灰共热来制取,不能使用该装置,错误;④CH≡CH是电石以水发生来制取,但是由于电石反应后呈糊状,乙醇不能使用该装置,错误;⑤H2是用Zn与稀盐酸发生反应来制取,符合该装置的使用,正确。(6)①NH3,③HCl在水中极容易溶解所以在尾气处理时为了防止倒吸现象的发生,应该使用倒扣的漏斗;②Cl2,④H2S在水中溶解度不大,应该用碱性溶液如NaOH溶液来吸收,导气管可以伸入到液面一下;(7)根据题意可知:25 mL NaOH溶液中NaOH的物质的量与产生的碳酸钠的物质的量相等,n(NaOH)= (1.44 g / mL ×25 mL ×40%)÷40g/mol=0.36mol,c(Na2CO3)= n(Na2CO3)÷V=0.36mol÷0.05L=7.2mol/L.
考点:考查物质的制取方法、装置气密性的检查、试剂的选择及作用、尾气处理方法、物质的量浓度的计算的知识。


科目:高中化学 来源:2013-2014福建安溪一中、惠安一中、养正中学下学期期中高二化学(解析版) 题型:选择题
下列关于化学反应的自发性叙述中正确的是 ( )
A.焓变小于0而熵变大于0的反应肯定是自发的
B.焓变和熵变都小于0的反应肯定是自发的
C.焓变和熵变都大于0的反应肯定是自发的
D.熵变小于0而焓变大于0的反应肯定是自发的
查看答案和解析>>
科目:高中化学 来源:2013-2014甘肃省高一下学期期末考试化学试卷(解析版) 题型:选择题
四种短周期元素在周期表中的位置如图,其中只有M为金属元素。下列说法不正确的是( )

| Y | Z | |
M | X |
| |
A.原子半径Z<M
B.Y的最高价氧化物对应水化物的酸性比X 的弱
C.X 的最简单气态氢化物的热稳定性比Z的小
D.Z位于元素周期表中第2 周期、第ⅥA族
查看答案和解析>>
科目:高中化学 来源:2013-2014甘肃省高一下学期期末考试化学试卷(解析版) 题型:选择题
某有机化合物6.2 g在氧气中完全燃烧,只生成8.8 g CO2和5.4 g H2O。下列说法正确的是( )
A.该化合物仅含碳、氢两种元素
B.该化合物中碳、氢原子个数比为1:4
C.无法确定该化合物是否含有氧元素
D.该化合物中一定含有氧元素
查看答案和解析>>
科目:高中化学 来源:2013-2014甘肃省高一下学期期末考试化学试卷(解析版) 题型:选择题
X元素的阳离子与Y的阴离子具有相同的核外电子排布,则下列比较中正确的是( )
A.原子序数: X<Y B.原子半径:X<Y
C.离子半径:X>Y D.原子最外层电子数:X<Y
查看答案和解析>>
科目:高中化学 来源:2013-2014甘肃省武威市高二下学期期末考试化学(理)试卷(解析版) 题型:选择题
要使含有Ba2+、Al3+、Cu2+、Mg2+、Ag+等离子的溶液中的各离子逐一形成沉淀析出,下列所选择的试剂及加入试剂的顺序正确的是 ( )
A.H2SO4—HCl—H2S—NaOH—CO2 B.HCl—H2SO4—Na2S—NaOH—CO2
C.NaCl—Na2SO4—Na2S—NaOH—CH3COOH D.Na2S—Na2SO4—NaCl—NaOH—HCl
查看答案和解析>>
科目:高中化学 来源:2013-2014甘肃省武威市高二下学期期末考试化学(理)试卷(解析版) 题型:选择题
下列化合物分子中的所有原子都处于同一平面的是 ( )
A.乙烷 B.对二甲苯 C.氯乙烯 D.丙烯
查看答案和解析>>
科目:高中化学 来源:2013-2014甘肃省武威市高一下学期期末考试化学(理)试卷(解析版) 题型:选择题
根据下表中烃的分子式排列规律,判断空格中烃的同分异构体数目是( )
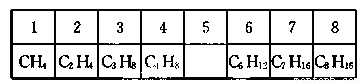
A.3 B.4 C.5 D.6
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com