
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
| 750℃ |
| 750℃ |
| 物质 | 溶解度/(g/100g水) | ||
| 0°C | 40°C | 80°C | |
| KCl | 28 | 40.1 | 51.3 |
| NaCl | 35.7 | 36.4 | 38 |
| K2Cr2O7 | 4.7 | 26.3 | 73 |
| Na2Cr2O7 | 163 | 215 | 376 |
| 26m |
| 17n |
| 26m |
| 17n |
查看答案和解析>>
科目:高中化学 来源:上海交通大学附中2009学年度第一学期高三摸底(化学) 题型:058
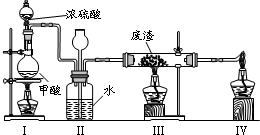
已知甲酸经浓硫酸加热脱水可制得CO,以下试剂和仪器(酒精灯未画出,仪器可重复使用)用于测定当CO气流通过Fe2O3粉末后,发生反应的CO在CO总量中所占的百分比.
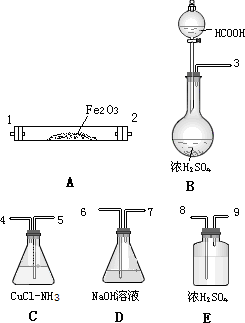
(1)氯化亚铜和氨水溶液吸收CO,实验装置合理的连接顺序自左至右为(填装置接口编号,空格不一定填满)
( )( )( )( )( )( )( )( )( )( )( )( )
(2)装置C和D的顺序不能颠倒,原因是________.
(3)装置B的反应中,浓硫酸是________.
a.吸水剂 b.脱水剂 c.氧化剂
(4)设装置C、D的增重为Δm(C)、Δm(D),发生反应的CO在CO总量中所占的质量分数(CO%)可表示为:CO%=________
如装置D、E的顺序颠倒,将使实验结果CO%________.(填增大、减小或不变)
(5)已知草酸(H2C2O4)有下列反应:H2C2O4(固)![]() CO+CO2+H2O
CO+CO2+H2O
用草酸热分解代替装置B进行上述实验,下列判断正确的是________.
a.不可行
b.增加CO2吸收装置也可行
c.不必增加任何装置也可行
查看答案和解析>>
科目:高中化学 来源:2013-2014学年江西省高三第四次模考化学试卷(解析版) 题型:填空题
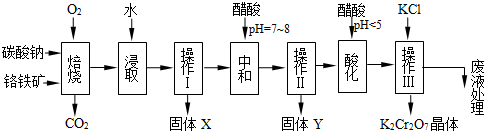
铬铁矿的主要成分可表示为FeO·Cr2O3,还含有MgO、Al2O3、Fe2O3等杂质,以下是以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的流程图:

已知:①4FeO·Cr2O3+ 8Na2CO3+
7O2 8Na2CrO4
+ 2 Fe2O3 + 8CO2↑;
8Na2CrO4
+ 2 Fe2O3 + 8CO2↑;
②Na2CO3
+ Al2O3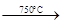 2NaAlO2
+ CO2↑;③ Cr2O72-+ H2O
2NaAlO2
+ CO2↑;③ Cr2O72-+ H2O 2CrO42- +
2H+
2CrO42- +
2H+
根据题意回答下列问题:
(1)固体X中主要含有_________(填写化学式);要检测酸化操作中溶液的pH是否等于4.5,应该使用__________(填写仪器或试剂名称)。
(2)酸化步骤用醋酸调节溶液pH<5,其目的是_________________________________。
(3)操作Ⅲ有多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体、蒸发浓缩、 、过滤、_______、干燥。
(4)下表是相关物质的溶解度数据,操作Ⅲ发生反应的化学方程式是:Na2Cr2O7+2KCl → K2Cr2O7↓+2NaCl。该反应在溶液中能发生的理由是_______________。
|
物质 |
溶解度/(g/100g水) |
||
|
0°C |
40°C |
80°C |
|
|
KCl |
28 |
40.1 |
51.3 |
|
NaCl |
35.7 |
36.4 |
38 |
|
K2Cr2O7 |
4.7 |
26.3 |
73 |
|
Na2Cr2O7 |
163 |
215 |
376 |
(5)副产品Y主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,精确分析Y中氢氧化铝含量是称取n g样品,加入过量______(填写试剂)、溶解、过滤、再______(填写试剂)、……灼烧、冷却、称量,得干燥固体m g 。计算样品中氢氧化铝的质量分数为_______(用含m、n的代数式表示)。
(6)六价铬有毒,而Cr3+相对安全。工业含铬(CrO3)废渣无害化处理的方法之一是干法解毒,用煤不完全燃烧生成的CO还原CrO3。在实验室中模拟这一过程的装置如下:
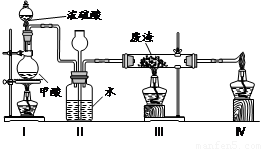
CO由甲酸脱水制得;实验结束时熄灭酒精灯的顺序是_________________________。
查看答案和解析>>
科目:高中化学 来源:浦东新区二模 题型:问答题
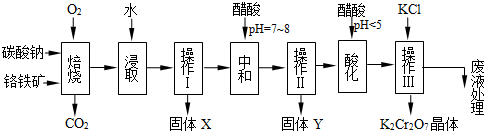
| 750℃ |
| 750℃ |
| 物质 | 溶解度/(g/100g水) | ||
| 0°C | 40°C | 80°C | |
| KCl | 28 | 40.1 | 51.3 |
| NaCl | 35.7 | 36.4 | 38 |
| K2Cr2O7 | 4.7 | 26.3 | 73 |
| Na2Cr2O7 | 163 | 215 | 376 |
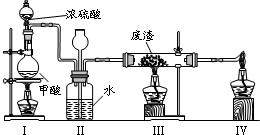
查看答案和解析>>
科目:高中化学 来源: 题型:
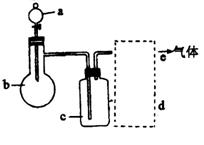
(1)在下表中填入最合适的试剂:
要制取的气体 | a | B | c | d |
C2H2 |
| 电石 | NaOH溶液 | 碱石灰 |
Cl2 | 浓盐酸 | MnO2 |
| 浓H2SO4 |
NO | 稀硝酸 | ①CaCO3②铜屑 |
| 固体P2O5 |
CO |
|
| NaOH溶液 | 浓H2SO4 |
(2)制取C2H2时,仪器C中NaOH溶液的作用是________________。
(3)制取Cl2时,必须处理多余的Cl2,其简易的处理方法是____________,写出上述方法对应的离子方程式___________。
(4)制取NO时,加入CaCO3的作用是____________。
(5)请在给出的实验装置基础上,进行改进,以证明浓硫酸使甲酸脱水时,既制得了CO,同时又产生了少量CO2,简述一种合理的实验改进方法:
答:______________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com