
已知:某温度时,Ksp(AgCl)=1.8×10-10 mol2·L-2,Ksp(Ag2CrO4)=1.1×10-12 mol3·L-3。
试求:
(1)此温度下AgCl饱和溶液和Ag2CrO4饱和溶液的物质的量浓度,并比较两者的大小。
(2)此温度下,在0.010 mol·L-1的AgNO3溶液中,AgCl与Ag2CrO4分别能达到的最大物质的量浓度,并比较两者的大小。
(1)AgCl(s)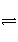
 Ag+(aq)+Cl-(aq)
Ag+(aq)+Cl-(aq)
[AgCl]= =
=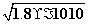 mol·L-1
mol·L-1
=1.3×10-5 mol·L-1
Ag2CrO4(s)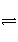
 2Ag+(aq)+CrO
2Ag+(aq)+CrO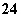 (aq)
(aq)
2x x
(2x)2·x=Ksp
[Ag2CrO4]= =
= mol·L-1=6.5×10-5 mol·L-1
mol·L-1=6.5×10-5 mol·L-1
所以[AgCl]<[Ag2CrO4]
(2)在0.010 mol·L-1 AgNO3溶液中,
[Ag+]=0.010 mol·L-1
AgCl(s)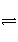
 Ag+(aq)+Cl-(aq)
Ag+(aq)+Cl-(aq)
溶解平衡时:0.010+x x
(0.010+x)·x=1.8×10-10
因为x很小,0.010+x≈0.010
x=1.8×10-8 mol·L-1
[AgCl]=1.8×10-8 mol·L-1
Ag2CrO4(s)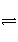
 2Ag+(aq)+CrO
2Ag+(aq)+CrO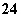 (aq)
(aq)
溶解平衡时: 0.010+2x x
(0.010+2x)2·x=1.1×10-12
因为x很小,0.010+2x≈0.010
x=1.1×10-8 mol·L-1
所以[Ag2CrO4]=1.1×10-8 mol·L-1
所以[AgCl]>[Ag2CrO4]


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案科目:高中化学 来源: 题型:
已知SiO2、SO2、CO2都是酸性氧化物,化学性质具有一定的相似性;Mg和Na的化学性质也具有一定的相似性(提示:2Mg+CO2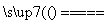 2MgO+C)。
2MgO+C)。
用如图所示的装置 进行Mg和SO2的实验:
进行Mg和SO2的实验:
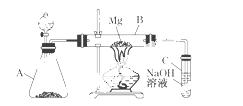
(1)选择制取SO2的合适试剂________.
①10%的H2SO4溶液;②80%的H2SO4溶液;③Na2SO 3固体;④CaSO3固体
3固体;④CaSO3固体
(2)写出装置B中发生的主要反应的化学方程式:_______________________
___________________________________________________________________.
(3)你认为该装置是否有不足之处?________,如果有,请列出两点:
________________________________________________________________________
_ _______________________________________________________________________.
_______________________________________________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:25℃时,Ksp[Mg(OH)2]=5.61×10-12 mol3·L-3,Ksp[MgF2]=7.42×10-11 mol3·L-3。下列说法正确的是( )
A.25℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的[Mg2+]大
B.25℃时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,[Mg2+]增大
C.25℃时,Mg(OH)2固体在20 mL 0.01 mol·L-1氨水中的Ksp比在20 mL 0.01 mol·L-1 NH4Cl溶液中的Ksp小
D.25℃时,在Mg(OH)2的悬浊液中加入NaF溶液后, Mg(OH)2不可能转化为MgF2
查看答案和解析>>
科目:高中化学 来源: 题型:
已知Ag2SO4的Ksp为2.0×10-5 mol3·L-3,将适量Ag2SO4固体溶于100 mL水中至刚好饱和,该过程中Ag+和SO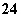 浓度随时间变化关系如图所示[饱和Ag2SO4溶液中[Ag+]=0.034 mol·L-1]。若t1时刻在上述体系中加入100 mL 0.020 mol·L-1 Na2SO4溶液,下列示意图中,能正确表示t1时刻后Ag+和SO
浓度随时间变化关系如图所示[饱和Ag2SO4溶液中[Ag+]=0.034 mol·L-1]。若t1时刻在上述体系中加入100 mL 0.020 mol·L-1 Na2SO4溶液,下列示意图中,能正确表示t1时刻后Ag+和SO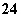 浓度随时间变化关系的是( )
浓度随时间变化关系的是( )
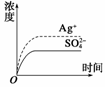
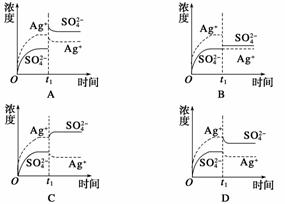
查看答案和解析>>
科目:高中化学 来源: 题型:
用铂电极(惰性)电解下列溶液时,阴极和阳极上的主要产物分别是H2和O2的是( )
A.稀NaOH溶液 B.HCl溶液
C.CuSO4溶液 D.酸性AgNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
写出用惰性电极电解下列电解质溶液的电极反应式及电解反应的化学方程式
(1)Ba(OH)2:____________________________________________________________;
(2)Na2CO3: __________________________________________________________;
(3)KCl: ____________________________________________________________;
(4)AgNO3: ___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知0.1 mol·L-1的二元酸H2A溶液的pH=4,则下列说法中正确的是( )
A.在Na2A、NaHA两溶液中,离子种类不相同
B.在溶质物质的量相等的Na2A、NaHA两溶液中,阴离子总数相等
C.在NaHA溶液中一定有[Na+]+[H+]=[HA-]+[OH-]+2[A2-]
D.在Na2A溶液中一定有[Na+]>[A2-]>[H+]>[OH-]
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下,体积为2 L的密闭容器中A、B、C三种气体的起始浓度和平衡浓度如下表:
| 物质 | A | B | C |
| 初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
| 平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
下列说法中正确的是( )
A.发生的反应可表示为A+B2C
B.反应达到平衡时B的转化率为25%
C.若起始时密闭容器中有0.1 mol A、0.1 mol B、0.2 mol C时,反应达平衡时,c(A)=0.05 mol·L-1
D.改变起始时容器中各气体的物质的量,可以改变此反应的平衡常数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com