
【题目】用某仪器量一液体体积时,平视时体积为V1ml,仰视读数为V2ml,俯视读数为V3ml,若V3>V1>V2,则所使用的仪器可能是 ( )
A. 容量瓶 B. 量筒 C. 碱式滴定管 D. 以上仪器均可
科目:高中化学 来源: 题型:
【题目】某温度下,在体积不变的容器中进行反应:CO(g)+2H2(g) ![]() CH3OH(g) △H1=-90.7 kJmol-1。已知反应的起始浓度分别为:c(CO)=1 mol/L,c(H2)=2.4 mol/L;5 min后反应达平衡,此时CO的转化率为50%。则下列说法正确的是:( )
CH3OH(g) △H1=-90.7 kJmol-1。已知反应的起始浓度分别为:c(CO)=1 mol/L,c(H2)=2.4 mol/L;5 min后反应达平衡,此时CO的转化率为50%。则下列说法正确的是:( )
A.该反应属于熵增放热反应,一定能自发进行
B.5 min内H2的平均反应速率为0.1 mol/(L·min)
C.若该温度下,反应物的起始浓度c(CO)=4 mol/L,c(H2)=a mol/L,达到平衡后,c(CH3OH)=2 mol/L,则a=5.4
D.其它条件不变的情况下,加入催化剂可提高CO的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关丙烯酸(CH2=CHCOOH)的说法正确的是
A. 丙烯酸使溴水褪色属于氧化反应
B. 丙烯酸能发生加成反应但不能发生取代反应
C. 丙烯酸分子中所有碳原子不可能处于同一平面
D. 反应 CH2=CHCOOH+H2![]() CH3CH2COOH的原子利用率为100%
CH3CH2COOH的原子利用率为100%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2H(g)+Y(g)![]() 2I(g)反应,在t℃时,在一压强恒定的密闭容器中,加入4 mol H和2 mol Y反应,达到平衡后,Y剩余0.2 mol。若在上面的平衡体系中,再加入1 mol气态的I物质,t ℃时达到新的平衡,此时H物质的物质的量n(H)为( )
2I(g)反应,在t℃时,在一压强恒定的密闭容器中,加入4 mol H和2 mol Y反应,达到平衡后,Y剩余0.2 mol。若在上面的平衡体系中,再加入1 mol气态的I物质,t ℃时达到新的平衡,此时H物质的物质的量n(H)为( )
A.0.2mol B.0.5 mol C.0.6 mol D.0.8 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(NOC1)的沸点为-5.5℃,具有刺鼻恶臭味,在潮湿空气中易水解,溶于浓硫酸,是而机合成中的重要试剂。某同学用下图装置,由NO与干燥纯净的Cl2反应制备NOCl。

己知:①Cl2沸点为-34.6℃,NO2Cl沸点为-15℃
②2NO+Cl2= 2NOC1![]() 2NO2 + Cl2=2NO2C1
2NO2 + Cl2=2NO2C1
回答下列问题:
(1)铜与稀硝酸反应的化学方程式为_______________;装置A中设计了可上下移动的铜丝,其优点是_____________________。
(2)上图中实验装置的连接顺序为:a→__________________。
(3)实验时,先制取氯气使充满除A、B、C外的整套装置,目的是______________;
装置中充满氯气后,下—步是制取NO,具体操作是_______________;
E中冰盐水的温度可低至-22℃,其作用是_______________。
(4)该同学的实验设计可能的不足之处是__________________(答出一条即可)。
(5)若无C装置,则不利于NOCl的制备,主要原因是_________(用化学方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(11分)在2L密闭容器内,800℃时反应:2NO(g)+O2(g) ![]() 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.01 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)达平衡的时间是 ,理由是 。
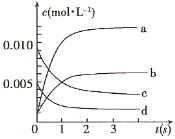
(2)右图中表示NO2的变化的曲线是 。用O2表示从0~2 s内该反应的平均速率v= 。
(3)能说明该反应已达到平衡状态的是 。
a.v(NO2) = 2v(O2) b.容器内各物质的浓度保持不变
c.v逆(NO) = 2v正(O2) d.达到化学平衡时,NO将完全转化为NO2
(4)能增大该反应的反应速率是 。
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能把Na2SO4、NH4NO3、KNO3、(NH4)SO4四瓶无色溶液加以区别的一种试剂是(必要时可以加热)
A. BaCl2 B. NaOH C. Ba(OH)2 D. AgNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以NA表示阿伏加德罗常数,则关于热化学方程式:
C2H2(g)+![]() O2(g)===2CO2(g)+H2O(l) ΔH=-1300 kJ/mol的说法中,正确的是( )
O2(g)===2CO2(g)+H2O(l) ΔH=-1300 kJ/mol的说法中,正确的是( )
A. 当有6 NA个电子转移时,该反应放出1300 kJ的能量
B. 当有1NA个水分子生成且为液体时,吸收1300 kJ的能量
C. 当有4NA个碳氧共用电子对生成时,放出1300 kJ的能量
D. 当有8NA个碳氧共用电子对生成时,放出1300 kJ的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,在20.0mL0.10 mol L–1氨水中滴入0.10 mol L–1的盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知0.10 mol L–1氨水的电离度为1.32%,下列有关叙述正确的是

A.该滴定过程应该选择酚酞作为指示剂
B.M点对应的盐酸体积为20.0mL
C.M点处的溶液中c(NH4+)=c(Cl-)=c(H+)=c(OH-)
D.N点处的溶液中pH<12
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com