
为除去粗盐中含有的Ca2+、Mg2+、Fe3+、![]() 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):称取粗盐
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):称取粗盐![]() 滤液
滤液![]()
![]() 精盐.
精盐.
(1)判断BaCl2已过量的方法是________.
(2)第④步中相关的离子方程式是________.
(3)若先用盐酸调pH再过滤,将对实验结果产生影响,其原因是________.
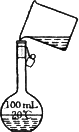
(4)为检验精盐纯度,需配制150 mL 0.2 mol·L-1 NaCl(精盐)溶液,如图是该同学转移溶液的示意图,图中的错误是________.
|
答案:(1)取第②步后的上层清液1~2滴于点滴板上,再滴入1~2滴BaCl2溶液,若溶液未变浑浊,表明BaCl2已过量. (2)Ca2++ (3)先加HCl会有少量Mg(OH)2、Fe(OH)3、CaCO3、BaCO3溶解,从而影响制得精盐的纯度. (4)未用玻璃棒引流,未采用150 mL容量瓶. 解析:加入BaCl2、NaOH、Na2CO3等沉淀剂后,产生BaSO4、Fe(OH)3、Mg(OH)2、BaCO3、CaCO3沉淀,还有过量Na2CO3,需加入HCl使Na2CO3转变成NaCl.但若先加HCl再过滤,Mg(OH)2、Fe(OH)3、BaCO3、CaCO3都可能溶解,造成产品纯度不高. 评注:点滴板是一种用于试剂检测的仪器,其优点是使用方便,节约试剂(药品). |


 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
三种物质的溶解度(20℃)如表所示,下列说法正确的是( )
|
查看答案和解析>>
科目:高中化学 来源: 题型:
(5分)海水是一种重要的自然资源。以下是我市对海水资源的部分利用。
(1)从海水中获得氯化钠。将海水进行 可得到粗盐;为除去粗盐中含有的SO42-、Ca2+、Mg2+等杂质,有如下操作:①溶解;②加过量的Na2CO3溶液; ③加过量的BaCl2溶液;④加适量的盐酸;⑤加过量NaOH溶液;⑥蒸发结晶;⑦过滤。正确的操作顺序是_________________。(用序号填一种合理组合)。
上述过程中,沉淀B与试剂C发生的是中和反应,则沉淀B的化学式为__________,
由无水MgCl2制取Mg的化学方程式为_____________________________________。海
水本身就是含有MgCl2的溶液,它与通过步骤①、②得到的MgCl2溶液有何不同:___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2012届黑龙江大庆市三十二中高三毕业班联考化学试卷 题型:填空题
(5分)海水是一种重要的自然资源。以下是我市对海水资源的部分利用。
(1)从海水中获得氯化钠。将海水进行 可得到粗盐;为除去粗盐中含有的SO42-、Ca2+、Mg2+等杂质,有如下操作:①溶解;②加过量的Na2CO3溶液; ③加过量的BaCl2溶液;④加适量的盐酸;⑤加过量NaOH溶液;⑥蒸发结晶;⑦过滤。正确的操作顺序是_________________。(用序号填一种合理组合)。 上述过程中,沉淀B与试剂C发生的是中和反应,则沉淀B的化学式为__________,
上述过程中,沉淀B与试剂C发生的是中和反应,则沉淀B的化学式为__________,
由无水MgCl2制取Mg的化学方程式为_____________________________________。海
水本身就是含有MgCl2的溶液,它与通过步骤①、②得到的MgCl2溶液有何不同:___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年黑龙江大庆市高三毕业班联考化学试卷 题型:填空题
(5分)海水是一种重要的自然资源。以下是我市对海水资源的部分利用。
(1)从海水中获得氯化钠。将海水进行 可得到粗盐;为除去粗盐中含有的SO42-、Ca2+、Mg2+等杂质,有如下操作:①溶解;②加过量的Na2CO3溶液; ③加过量的BaCl2溶液;④加适量的盐酸;⑤加过量NaOH溶液;⑥蒸发结晶;⑦过滤。正确的操作顺序是_________________。(用序号填一种合理组合)。
 上述过程中,沉淀B与试剂C发生的是中和反应,则沉淀B的化学式为__________,
上述过程中,沉淀B与试剂C发生的是中和反应,则沉淀B的化学式为__________,
由无水MgCl2制取Mg的化学方程式为_____________________________________。海
水本身就是含有MgCl2的溶液,它与通过步骤①、②得到的MgCl2溶液有何不同:___________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com