
氮可以形成多种离子,如N3-,NH2-,N3-,NH4+,N2H5+,N2H62+等,已知N2H5+
与N2H62+是由中性分子结合质子形成的,类似于NH4+,因此有类似于 NH4+的性质。
⑴写出N2H62+在碱性溶液中反应的离子方程式 。
⑵NH2-的电子式为 。
⑶N3-有 个电子。
⑷写出二种由多个原子组成的含有与N3-电子数相同的物质的化学式 、 。
⑸等电子数的微粒往往具有相似的结构,试预测N3—的构型 。
⑹据报道,美国科学家卡尔·克里斯特于1998年11月合成了一种名为“N5”的物质,由于其具有极强的爆炸性,又称为“盐粒炸弹”。迄今为止,人们对它的结构尚不清楚,只知道“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排成V形。如果5个N结合后都达到8电子结构,且含有2个N≡N键。则“N5”分子碎片所带电荷是 。
⑴N2H62++2OH-=N2H4+2H2O ⑵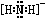 ⑶22
⑶22
⑷N2O CO2 CNO- BeF2 CaH2 C3H4等 ⑸直线型 ⑹一个单位正电荷
【解析】
试题分析:⑴NH4+与碱反应的离子方程式为:NH4++OH-=NH3+H2O。由于NH4+ 与N2H62+结构相似,所以N2H62+在碱性溶液中反应的离子方程式为N2H62++2OH-=N2H4+2H2O 。⑵NH2-是NH3失去质子后形成的。所以NH2-的电子式为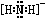 。⑶N是7号元素,所以N3-有22个电子。⑷由多个原子组成的含有与N3-电子数相同的物质有N2O 、 CO2、 CNO-、BeF2、CaH2 、C3H4等。⑸等电子数的微粒往往具有相似的结构,由于CO2与N3—是等电子体。所以N3—的构型是直线型。⑹其结构是对称的,5个N排成V形。如果5个N结合后都达到8电子结构,且含有2个N≡N键。其结构为
。⑶N是7号元素,所以N3-有22个电子。⑷由多个原子组成的含有与N3-电子数相同的物质有N2O 、 CO2、 CNO-、BeF2、CaH2 、C3H4等。⑸等电子数的微粒往往具有相似的结构,由于CO2与N3—是等电子体。所以N3—的构型是直线型。⑹其结构是对称的,5个N排成V形。如果5个N结合后都达到8电子结构,且含有2个N≡N键。其结构为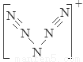 “N5”分子碎片所带电荷是一个单位正电荷。
“N5”分子碎片所带电荷是一个单位正电荷。
考点:考查氮元素形成的多种离子的结构与性质的知识。


 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源:2015届湖北省高三上学期起点考试化学试卷(解析版) 题型:选择题
下列有关实验操作中,正确的是
A.用试管取出试剂瓶中的NaOH溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中
B.银镜反应实验后的废液可先倒入水槽中,再用水冲入下水道
C.向试管中滴加液体时,胶头滴管必须紧贴试管内壁,避免液体溅出
D.用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中
查看答案和解析>>
科目:高中化学 来源:2015届湖北省新高三起点调研测试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.天然油脂的分子中含有酯基,属于酯类
B.煤经处理变为气体燃料的过程属于物理变化
C. A12O3可以与水反应得到其对应水化物 Al(OH)3
D.可以用加热使蛋白质变性的方法分离提纯蛋白质
查看答案和解析>>
科目:高中化学 来源:2015届湖北省高三上学期起点考试化学试卷(解析版) 题型:选择题
已知AgCl、AgBr的溶解度分别为1.5×10-4g、8.4×10-6 g(20℃)。将AgCl与AgBr的饱和溶液等体积混合,再加入足量的浓硝酸银溶液,发生的反应为( )。
A.只有AgBr沉淀生成 B. AgCl和AgBr沉淀等量生成
C. AgCl沉淀少于AgBr沉淀 D. AgCl沉淀多于AgBr沉淀
查看答案和解析>>
科目:高中化学 来源:2015届湖北省高三上学期起点考试化学试卷(解析版) 题型:选择题
下列实验能达到目的的是( )
|
|
|
|
用酒精萃取溴水中的溴 | 将硫酸铜溶液直接蒸干得到胆矾 | 说明2NO2(g) | 实验室制备Fe(OH)2 |
A | B | C | D |
查看答案和解析>>
科目:高中化学 来源:2015届湖北省孝感市七校联考高二下学期期中考试化学试卷(解析版) 题型:选择题
对充有氖气的霓虹灯管通电,灯管发出红色光。产生这一现象的主要原因( )
A.在电流的作用下,氖原子与构成灯管的物质发生反应
B.电子由基态向激发态跃迁时吸收除红光以外的光线
C.氖原子获得电子后转变成发出红光的物质
D.电子由激发态向基态跃迁时以光的形式释放能量
查看答案和解析>>
科目:高中化学 来源:2015届湖北省孝感市七校联考高二下学期期中考试化学试卷(解析版) 题型:选择题
实验测得 BeCl2为共价化合物,两个Be—Cl键间的夹角为180°。由此可见,BeCl2属于( )
A.由极性键构成的极性分子 B.由极性键构成的非极性分子
C.由非极性键构成的极性分子 D.由非极性键构成的非极性分子
查看答案和解析>>
科目:高中化学 来源:2015届浙江省协作体高考摸底测试理科综合化学试卷(解析版) 题型:选择题
化学与生活、社会密切相关。下列说法正确的是( )。
A.Si常用做信息高速公路的骨架—— 光导纤维的主要材料
B.近年来已发布“空气质量日报”,将CO2、NO2和可吸入颗粒物等列入了首要污染物
C.煤炭经气化、液化和干馏等过程,可获得清洁能源和重要的化工原料
D.SO2可以用来漂白纸浆、毛、丝、草帽辫、增白食品等
查看答案和解析>>
科目:高中化学 来源:2015届浙江省温州市十校联合体高三上学期期初联考化学试卷(解析版) 题型:选择题
根据下图海水综合利用的工业流程图,判断下列说法正确的是( )
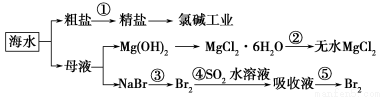
已知:MgCl2·6H2O受热生成Mg(OH)Cl和HCl气体等。
A.除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序为:NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸
B.在过程②中将MgCl2·6H2O灼烧即可制得无水MgCl2
C.从能量转换角度来看,氯碱工业中的电解饱和食盐水是一个将化学能转化为电能的过程
D.从第③步到第⑤步的目的是为了浓缩
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com