
(10分)固体碘在水中溶解度很小,实验室配制较浓的“碘水”时常将固体碘溶于一定浓度的KI溶液中。已知:I2与KI溶液发生如下反应:I2(aq)+I¯(aq) ![]() I3¯(aq),该反应平衡常数随温度升高而减小。
I3¯(aq),该反应平衡常数随温度升高而减小。
(1)下列有关说法正确的是 ▲ 。
 A.反应:I2(aq)+I¯(aq)
A.反应:I2(aq)+I¯(aq) ![]() I3¯(aq)的△H >0
I3¯(aq)的△H >0
B. I3¯的平衡浓度[c(I3¯)]与温度T的关系如右图
C.在I2的KI水溶液中加入少量的NaOH(s)或FeCl3(s)均可使溶液中c(I3¯)减小
D.依此原理, Cl2在一定浓度的NaCl溶液中溶解度增大
(2)t℃时,将0.850 mol KI固体和0.820 mol 固体I2溶于水配成1000 mL KI-I2的水溶液,经测定该溶液中c(I2)= 0.0200 mol·L-1。
①t℃时,计算反应I2(aq)+I¯(aq) ![]() I3¯(aq)的平衡常数K(要求写出计算过程)。
I3¯(aq)的平衡常数K(要求写出计算过程)。
▲
②已知:2Na2S2O3+I2=Na2S4O6+2NaI。若取上述所配溶液2.0 mL于锥形瓶中加水稀释后,再加两滴淀粉溶液,然后用0.100 mol·L-1 Na2S2O3标准溶液进行滴定,计算滴定终点时所消耗的Na2S2O3标准溶液的体积(要求写出计算过程)。
▲
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案科目:高中化学 来源: 题型:

| ||
| △ |
| ||
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:
I、氨气是一种重要化合物,在工农业生产、生活中有着重要应用。
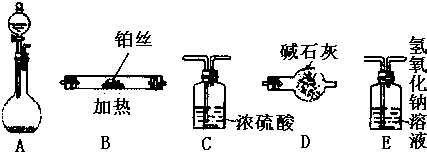
(1)下图烧瓶中盛有Na2O2固体,分液漏斗中盛有浓氨水,利用图示仪器装置(加热及夹持固定装置均已略去)进行氨的催化氧化实验。请根据下列要求回答问题:

①请选择实验装置,按气流方向从左到右连接顺序是(填字母)( )→( )→( )→E;
②试管B中的反应方程式为 ;
II、①分别将氯气和二氧化硫通入品红溶液中,可观察到红色都褪去,该过程中分别体现了氯气的 性、二氧化硫的 性。
②一定条件下,向碘水中通入足量氯气,完全反应后再滴加淀粉溶液无明显现象。若原有10.0mL 1.0mo1·![]() 的碘水,反应中共转移了0.1mo1电子,则该反应的离子方程式为:
的碘水,反应中共转移了0.1mo1电子,则该反应的离子方程式为:
。
III、为了探究NO做催化剂参与的硫酸型酸雨的形成,在烧瓶中充入含有少量NO的SO2气体,慢慢通入O2,该过程中发生反应化学方程式为 、 ,再喷射适量蒸馏水即得硫酸型酸雨 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com