
【题目】由以下粒子结构示意图得出的结论正确的是( ) 
A.④表示的是阳离子
B.①③属于同种元素,②④属于另一种元素
C.②④形成的化合物是Al2O3
D.①③的化学性质相似
【答案】A
【解析】解:A、④质子数=13,核外电子数=10,质子数>核外电子数,为阳离子,故A正确; B、元素是质子数(即核电荷数)相同的一类原子的总称,决定元素种类的是质子数(即核电荷数),同种元素的粒子是质子数相同,①③的质子数相同,属于同种元素;②、④的核内质子数分别是16、13,属于另外两种元素,故B错误;
C、②、④的核内质子数分别是16、13,分别为硫元素、铝元素;硫原子的最外层电子数为6,在化学反应中易得到2个电子而形成2个单位负电荷的阴离子,化合价的数值等于离子所带电荷的数值,且符号一致,则该元素的化合价为﹣2价;④是带3个单位正电荷的阳离子,化合价的数值等于离子所带电荷的数值,且符号一致,则该元素的化合价为+3价;铝元素显+3价,硫元素显﹣2价,镁和氯组成化合物的化学式为Al2S3 , 故C错误;
D、决定元素化学性质的是原子的最外层电子数,①③的最外层电子数不同,化学性质不相似,故D错误;
故选A.


 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
【题目】下列有关品格能的说法错误的是( )
A.晶格能越大,离子晶体越稳定
B.晶格能越大,离子晶体的硬度越小
C.晶格能越大,离子晶体的能量越低
D.晶格能越大,离子晶体的熔点越高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】构成细胞的化学元素没有一种是生命物质所特有的这个事实说明
A. 生物体是由无机物组成的
B. 生物与非生物完全相同
C. 生物界与非生物界具有统一性
D. 生物与非生物完全不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】部分短周期元素原子半径的相对大小、最高正价或最低负价随原子序数的变化关系如图所示,下列说法正确的是
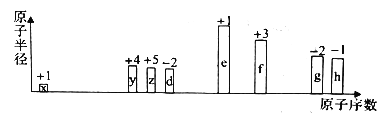
A. 离子半径的大小顺序:d
B. 与x形成简单化合物的沸点:y>z>d
C. 除去实验后试管中残留的g单质,可用热的氢氧化钠溶液
D. g、h的氧化物对应的水化物的酸性:h>g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学方程式书写正确的是( )
A.CO2+H2O+CaCl2═2HCl+CaCO3↓
B.2NaCl+MgSO4═Na2SO4+MgCl2
C.2HgO═2Hg+O2
D.2KOH+CO2═K2CO3+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电子工业中,常用氯化铁溶液作为印刷电路铜板蚀刻液。请按要求回答下列问题:
(1)若向氯化铁溶液中加入一定量的澄清石灰水,调节溶液pH,可得红褐色沉淀,该反应的离子方程式为:______________________________________,该过程中调节溶液的pH为5,则c(Fe3+)为:____________mol·L-1。(己知:Ksp[Fe(OH)3]= 4.0×10-38)
(2)某探究小组设计如下线路处理废液和资源回收:
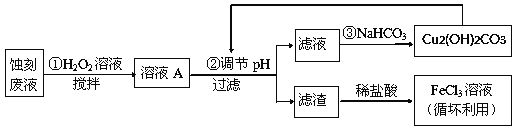
①用足量FeCl3溶液蚀刻铜板后的废液中含有的金属阳离子有:_______________。
②FeCl3蚀刻液中通常加入一定量的盐酸,其中加入盐酸的目的是:_________________。
③步骤①中加入H2O2溶液的目的是:______________________________________。
④已知:生成氢氧化物沉淀的pH
Cu(OH)2 | Fe(OH)2 | Fe(OH)3 | |
开始沉淀时 | 4.7 | 7.0 | 1.9 |
沉淀完全时 | 6.7 | 9.0 | 3.2 |
根据表中数据推测调节pH的范围是:________________。
⑤写出步骤②中生成CO2的离子方程式:__________(已知Cu2(OH)2CO3难溶于水)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法正确的是( )
A.聚乙烯可发生加成反应
B.石油干馏可得到汽油、煤油等
C.丁烷的沸点低于丙醇
D.苯不能使酸性高锰酸钾溶液褪色,所以苯不能发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某天然碱(纯净物)可看作由CO2和NaOH反应后的产物所组成。称取天然碱样品四份溶于水后,分别逐滴加入相同浓度的盐酸溶液30mL,产生CO2的体积(标准状况)如下表:
Ⅰ | Ⅱ | Ⅲ | Ⅳ | |
盐酸液的体积(mL) | 30 | 30 | 30 | 30 |
样品(g) | 2.26 | 3.39 | 5.65 | 6.78 |
二氧化碳的体积(mL) | 448 | 672 | 784 | 672 |
(1)由以上数据,可以推测用1.13g样品进行同样的实验时,产生CO2______mL(标准状况).
(2)另取2.26g天然碱样品于300℃加热分解至完全(300℃时NaCO3不分解),产生CO2 112mL(标准状况)和水0.45g,计算并确定该天然碱的化学式_________.
(3)依据上表所列数据以及天然碱的化学式,试求盐酸的浓度_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com