
【题目】SO2气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下两个化学反应:
①SO2+2Fe3++2H2O===SO42-+2Fe 2++4H+;
②Cr2O72-+6Fe2++14H+===2Cr3++6Fe3++7H2O。
下列有关说法不正确的是( )
A. SO2发生氧化反应
B. 若有13.44 L SO2(标准状况)参加反应,则最终消耗0.4mol K2Cr2O7
C. 氧化性:SO42- < Fe3+ < Cr2O72-
D. 每0.2 mol K2Cr2O7参加反应,转移电子的数目为1.2NA
【答案】B
【解析】
在SO2+2Fe3++2H2O=SO42-+2Fe2++4H+中,S元素的化合价升高,Fe元素的化合价降低,在Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O中,Cr元素的化合价降低,Fe元素的化合价升高,再结合氧化还原反应的基本概念和规律分析判断。
A. 在SO2+2Fe3++2H2O=SO42-+2Fe2++4H+中,S元素的化合价升高,所以SO2为还原剂发生氧化反应,A项正确;
B. 若有13.44 L SO2(标准状况)参加反应,n(SO2)=13.44L÷22.4L/mol=0.6mol,由得失电子守恒可知,最终消耗K2Cr2O7的物质的量为![]() =0.2mol,B项错误;
=0.2mol,B项错误;
C.由氧化剂的氧化性大于氧化产物的氧化性可知,氧化性SO42- < Fe3+ < Cr2O72-,C项正确;
D.当1mol K2Cr2O7参加反应时,转移电子的物质的量为1mol×2×(6-3)=6mol,则每0.2 mol K2Cr2O7参加反应,转移电子的物质的量为0.2mol×6=1.2mol,数目为1.2NA,D项正确,答案选B。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】X、Y、Z、R、W为五种短周期元素。X原子最外层电子数是核外电子层数的3倍;Y最高正价与最低负价代数和为4;Z的单质常用于漂白工业;R是短周期元素中金属性最强的元素,W是生活中的常见金属,其氧化物常做耐高温材料。回答下列问题:
(1)Y元素的名称______,在周期表中的位于第三周期__________族
(2)W与Z单质化合得到的物质属于__________化合物(选填“离子”或“共价”),向其溶液中加入足量NaOH溶液,反应的离子方程式为______。
(3)工业上常用W单质与氨气在1700℃发生置换反应,生成一种最轻的气体和一种坚硬耐磨的固体,试写出该反应的化学方程式_________________________。
(4)化合物甲由元素X、R组成,甲能与水剧烈反应,并产生大量气泡,写出其化学反应方程式______,甲的电子式为_____________。
(5)为比较元素X和Y的非金属性强弱,下列方法不可行的是___。
a.比较这两种元素的常见单质的沸点
b.比较这两种元素的单质与氢气化合的难易
c.比较这两种元素的气态氢化物的稳定性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物X(分子式为C4H6O5)广泛存在于许多水果中,尤以苹果、葡萄、西瓜、山楂内为多。经测定该有机物具有下列性质(见下表)。请根据题目要求填空:
X的性质 | |
① | X与足量的金属钠反应产生氢气 |
② | X与醇或羧酸在浓硫酸加热条件下均能生成有香味的产物 |
③ | 在一定条件下X的分子内脱水产物(不是环状化合物)可与溴水发生加成反应 |
④ | 33.5gX与100mL的5mol/LNaOH溶液恰好完全中和 |
(1)X的可能结构简式I:________,Ⅱ:__________,Ⅲ:__________。
(2)在一定条件下有机物X可发生化学反应的类型有(填序号)__________。
A.水解反应 B.取代反应 C.加成反应 D.消去反应 E.加聚反应 F.中和反应
(3)下列物质与X互为同系物的是(填序号)_______,与X互为同分异构体的是(填序号)_______。
(a)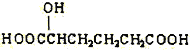 (b)
(b)![]()
(c)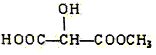 (d)H3COOC-COOCH3
(d)H3COOC-COOCH3
(e)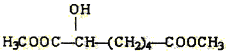 (f)
(f)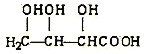
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、R、M、N为六种短周期元素,其原子半径和最外层电子数之间的关系如图所示。
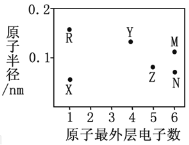
(1)M元素的原子核外有__________种能量不同的电子,有__________个未成对电子;Z元素在元素周期表中的位置是第______周期________族。
(2)N、R、X三种元素的原子可构成一种强碱性物质,该物质的电子式是___________;Y元素的氧化物是制造光纤的主要材料,该氧化物是________晶体(填晶体类型)。某化工生产的核心环节的反应为:2MN2(g) + N2(g) 2 MN3(g) + Q(Q>0)
(3)该反应的平衡常数表达式![]() __________________________;欲使K值变大,可采取的措施是__________________________。
__________________________;欲使K值变大,可采取的措施是__________________________。
(4)该反应达到平衡后,在其他条件不变的情况下,若使得容器的体积扩大为原来的两倍,则平衡____________________。(选填“正向移动”、“逆向移动”或“不移动”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.2mol某烃A在氧气中完全燃烧后,生成CO2和H2O各为0.4mol。将A通入溴的四氯化碳溶液中,溶液褪色。试回答:
(1)烃A的电子式为:___________________________。
(2)若取一定量的该烃A在一定量的氧气中燃烧后,生成CO2和H2O的物质的量分别为0.1mol和0.3mol,同时还有CO生成,则在燃烧时消耗标准状况下氧气的体积___________________L。
(3)将A通入溴的四氯化碳溶液中,生成的产物的名称为______________________________。
(4)可以用来除去乙烷中混有的A的试剂是______________(填序号)。
①水 ②氢气 ③溴水 ④酸性高锰酸钾溶液
(5)有机物B比A在分子组成上多一个CH2原子团,结构与A相似。写出B在一定条件下生成高分子化合物的化学方程式_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验过程如图所示:则图③的试管中的现象是
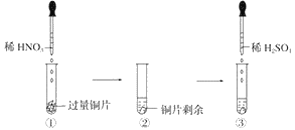
A. 无明显现象,因稀硫酸不与铜反应
B. 铜片溶解,产生无色气体,该气体遇到空气不变色
C. 铜片溶解,放出红棕色有刺激性气味的气体
D. 铜片溶解,产生无色气体,该气体在试管口变为红棕色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组通过查阅资料得知,CO2与Na2O2的反应需要在一定量水蒸气存在的条件下才能进行,于是他们设计了如图所示的装置对此问题进行探究,同时验证Na2O2与CO2反应的气体产物。

(1)写出装置A中有关反应的离子方程式:_________________,装置B中的试剂是____,装置E的作用是_____________。
(2)U形管C中的试剂是____。若要求根据装置D中的现象来确定CO2与Na2O2之间的反应是否需要在潮湿的条件下才能进行,对两个止水夹的操作方式为先打开K1,关闭K2,D中无明显现象;当打开K2,关闭K1,D中的现象为 ______________,则说明反应需要在潮湿条件下进行。
(3)检验气体产物的方法:用玻璃片在水里盖住集气瓶口,将集气瓶从水中取出,正放在实验台上,_______________。
(4)有人认为,经过较长时间反应后,装置D中生成的物质只有Na2CO3而没有NaOH。请设计一个方案证明此结论是正确的:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对于某些离子的检验及结论中一定正确的
A. 加入稀盐酸产生无色的气体,将气体通入澄清石灰水中,溶液变浑浊,一定有![]()
B. 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有![]()
C. 加入氢氧化钠溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,一定有![]()
D. 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com