
| A. | 若完全燃烧,1 mol雄酮(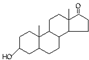 )比雌酮( )比雌酮(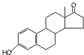 )多消耗2 mol O2 )多消耗2 mol O2 | |
| B. | 苯分子中的一个碳原子被一个氮原子代替,则新分子的式量为79 | |
| C. | 蔗糖、麦芽糖和乳糖的分子式都为C12H22O11,均能发生银镜反应 | |
| D. | 只用溴水一种试剂不能鉴别甲苯、己烯、乙醇、四氯化碳四种液体 |
分析 A.根据雄酮和雌酮的结构简式找出分子组成差别,然后求算出消耗氧气的多少;
B.碳原子能够结合4个H,氮原子只能结合3个H,再根据N、C的相对原子量判断新的分子的式量;
C.麦芽糖和乳糖为还原性糖,能够发生银镜反应,而蔗糖不具有还原性,不能发生银镜反应;
D.甲苯、己烯、四氯化碳、乙醇4种无色液体分别与溴水混合的现象为:分层后有色层在上层、溴水褪色、分层后有色层在下层、不反应不分层.
解答 解:A.对比雄酮和雌酮的结构可知,雌酮苯环,雄酮不含,雄酮比雌酮多1个C、8个H原子,所以雄酮比雌酮多消耗3mol O2,故A错误;
B.苯的相对分子量为78,苯分子中的一个碳原子被一个氮原子代替,N比C的相对原子量大2,而氢原子数目减少1,所以新的分子的式量为:78+2-1=79,故B正确;
C.蔗糖、麦芽糖和乳糖的分子式都为C12H22O11,其中麦芽糖和乳糖为还原性糖,二者能发生银镜反应,而蔗糖不具有还原性,不能发生银镜反应,故C错误;
D.甲苯、己烯、四氯化碳、乙醇4种无色液体分别与溴水混合的现象为:分层后有色层在上层、溴水褪色、分层后有色层在下层、不反应不分层,现象不相同,可以鉴别,故D错误.
故选B.
点评 本题考查了有机物结构与性质、有机反应的综合应用,题目难度中等,注意掌握常见有机物的组成、结构及具有的化学性质,选项B为易错点,注意分子式量的计算方法.


 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案科目:高中化学 来源: 题型:解答题
 与
与 
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放热91.5 kJ | B. | 放热183 kJ | C. | 吸热183 kJ | D. | 吸热91.5 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
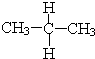 与
与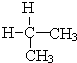 ⑦CH3CH3与
⑦CH3CH3与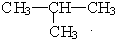
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl-、Br-、CrO42- | B. | CrO42-、Br-、Cl- | C. | Br-、Cl-、CrO42- | D. | Br-、CrO42-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 +3HNO3 $→_{△}^{浓硫酸}$
+3HNO3 $→_{△}^{浓硫酸}$ +3H2O.
+3H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 中国全运会期间,在济南市等主要街道上,出现了一座座拔地而起的立体花坛,4000万盆、上百种鲜花扮靓了济南街头.大量盆栽鲜花因施用了S-诱抗素制剂,得以保证鲜花盛开,S-诱抗素的分子结构如右图,下列关于该分子的说法正确的是( )
中国全运会期间,在济南市等主要街道上,出现了一座座拔地而起的立体花坛,4000万盆、上百种鲜花扮靓了济南街头.大量盆栽鲜花因施用了S-诱抗素制剂,得以保证鲜花盛开,S-诱抗素的分子结构如右图,下列关于该分子的说法正确的是( )| A. | 1mol该物质与足量的NaOH溶液反应最多消耗2mol NaOH | |
| B. | 该物质在Cu作催化剂条件下能被催化氧化 | |
| C. | 该物质能发生氧化、还原、取代反应 | |
| D. | 分别与足量的Na、NaHCO3 反应生成的气体在相同状况下体积比为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电池工作时,锌失去电子 | |
| B. | 电池正极的电极反应式为:2MnO2(s)+H2O(l)+2e-═Mn2O3(s)+2OH-(aq) | |
| C. | 电池工作时,电子由正极通过外电路流向负极 | |
| D. | 外电路中每通过0.1 mol电子,锌的质量理论上减小3.25 g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com