
科目:高中化学 来源:不详 题型:单选题
| A.浓硫酸与水 | B.生石灰与水 | C.熟石灰与水 | D.氯化钠与水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CH3CH2OH(g)+3H2O(g)发生的适宜条件,现改变氢碳比[n(H2)/n(CO2)]和温度等条件进行了如下实验:
CH3CH2OH(g)+3H2O(g)发生的适宜条件,现改变氢碳比[n(H2)/n(CO2)]和温度等条件进行了如下实验: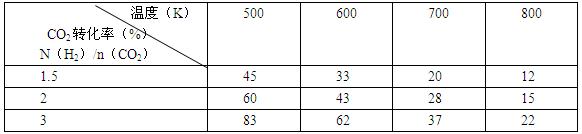
 CH3OH(g)+H2O(g)。2min时该反应达到平衡,测得CH3OH的物质的量浓度为0.2mol/L。下列说法正确的是 。
CH3OH(g)+H2O(g)。2min时该反应达到平衡,测得CH3OH的物质的量浓度为0.2mol/L。下列说法正确的是 。A.该反应的平衡常数表达式为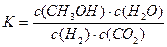 |
| B.CO2的平衡转化率为40% |
| C.2min内H2的平均反应速率为0.3mol/(L·min) |
| D.该反应达到平衡状态的标志是混合气体的密度不发生改变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CO(g)+H2O(g)。其化学平衡常数K和温度T的关系如下表:
CO(g)+H2O(g)。其化学平衡常数K和温度T的关系如下表:| T℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |

 ),容器内混合气体的密度 (填“增大”、“减小”或“不变”),气体平均相对分子质量 (填“增大”、“减小”或“不变”)。
),容器内混合气体的密度 (填“增大”、“减小”或“不变”),气体平均相对分子质量 (填“增大”、“减小”或“不变”)。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.AgCl难溶于水,溶液中没有Ag+和Cl- |
| B.自发过程将一定导致体系的熵值增大 |
| C.由能量判据和熵判据组合而成的复合判据,将更适合于所有过程的方向的判断 |
| D.增大反应物的浓度可增大单位体积活化分子百分数,从而使有效碰撞次数增多 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.热稳定性:Na2CO3 >NaHCO3 | B.溶解度:Na2CO3<NaHCO3 |
| C.与盐酸反应的速率:Na2CO3 <NaHCO3 | D.相对分子量:Na2CO3 >NaHCO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.已知2H2(g)+O2(g) ==2H2O(l);△H=-571.6kJ·mol-1,则H2的燃烧热为285.8kJ·mol-1 |
| B.已知4P(红磷,s)="=" P4(白磷,s);△H>0,则白磷比红磷稳定 |
| C.含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则稀醋酸和稀NaOH溶液反应的热化学方程式为: NaOH(aq)+CH3COOH(aq) ="=" CH3COONa(aq) + H2O(l) △H =-57.4kJ·mol-1 |
| D.已知2C(s)+2O2(g)=2CO2(g) △H1;2C(s)+O2(g)="2CO(g)" △H2,则△H1>△H2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com