
工业上制取冰晶石(Na3AlF6)的化学方程式如下:
2Al(OH)3+12HF+3Na2CO3=2Na3AlF6+3CO2↑+9H2O。根据题意完成下列填空:
⑴在上述反应的反应物和生成物中,CO2 的电子式 ,属于弱酸的电离方程式 。若0.1mol∙L-1的该弱酸溶液的pH为a,则该弱酸的电离度为 (用a表示)
⑵反应物中有两种元素在元素周期表中位置相邻,下列能判断它们的金属性或非金属性强弱的是 (选填编号)。
a.气态氢化物的稳定性 b.最高价氧化物对应水化物的酸性
c.单质与氢气反应的难易 d.单质与同浓度酸发生反应的快慢
⑶反应物中某些元素处于同一周期。它们最高价氧化物对应的水化物之间发生反应的离子方程式为 。
⑷Na2CO3俗称纯碱,属于 晶体。工业上制取纯碱的原料是 。
⑸F2能溶于NaOH溶液中生成OF2,写出该反应的化学方程式并配平
(1)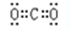 ,HF
,HF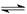 H++F-
10a+1×100% (2)ac
H++F-
10a+1×100% (2)ac
(3)Al(OH)3+OH-=AlO2-+2H2O
⑷离子 NH3、NaCl饱和溶液、CO2。
⑸2F2+2NaOH=2NaF+OF2+H2O
【解析】(1)CO2是含有极性键的共价化合物,电子式为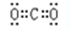 。HF是弱酸存在电离平衡,方程式为HF
。HF是弱酸存在电离平衡,方程式为HF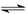 H++F-。pH=a,则氢离子浓度是10-amol/L,所以电离度
H++F-。pH=a,则氢离子浓度是10-amol/L,所以电离度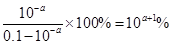
(2)两种元素分别是O和F,非金属性的比较规律:
1、由元素原子的氧化性判断:一般情况下,氧化性越强,对应非金属性越强。
2、由单质和酸或者和水的反应程度判断:反应越剧烈,非金属性越强。
3、由对应氢化物的稳定性判断:氢化物越稳定,非金属性越强。
4、由和氢气化合的难易程度判断:化合越容易,非金属性越强。
5、由最高价氧化物对应水化物的酸性来判断:酸性越强,非金属越强。(除氟元素之外)
6、由对应阴离子的还原性判断:还原性越强,对应非金属性越弱。
7、由置换反应判断:强置弱。〔若依据置换反应来说明元素的非金属性强弱,则非金属单质应做氧化剂,非金属单质做还原剂的置换反应不能作为比较非金属性强弱的依据〕
值得注意的是:氟元素没有正价态,故没有氟的含氧酸,所以最高价氧化物对应水合物的酸性最强的是高氯酸,而不是非金属性高于氯的氟元素!故规律5只适用于氟元素之外的非金属元素。
8、按元素周期律,同周期元素由左到右,随核电荷数的增加,非金属性增强;同主族元素由上到下,随核电荷数的增加,非金属性减弱。
据此可知选项ac正确,答案选ac。
(3)氢氧化铝是两性氢氧化物,能和氢氧化钠反应,方程式为Al(OH)3+OH-=AlO2-+2H2O。
(4)碳酸钠是离子化合物,形成的晶体是离子晶体,制取碳酸钠的原料是NH3、NaCl饱和溶液、CO2。
(5)根据原子守恒可知,另外的生成物是氟化钠和水,方程式为2F2+2NaOH=2NaF+OF2+H2O。


科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
(7分)工业上制取冰晶石(Na3AlF6)的化学方程式如下:
2Al(OH)3+ 12HF+ 3Na2CO3=2Na3AlF6+3CO2↑+ 9H2O
根据题意完成下列填空:
(1)在上述反应的反应物和生成物中, 属于弱酸,电离方程式 。
(2)反应物中有两种元素在元素周期表中位置相邻,下列能判断它们的金属性或非金属性强弱的是 (选填编号)。
a.气态氢化物的稳定性 b.最高价氧化物对应水化物的酸性
c.单质与氢气反应的难易 d.单质与同浓度酸发生反应的快慢
(3)反应物中某些元素处于同一周期。它们最高价氧化物对应的水化物之间发生反应的离子方程式为 。
(4) Na2CO3俗称纯碱,属于 (填离子或共价)化合物。其中含有的化学键是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(7分)工业上制取冰晶石(Na3AlF6)的化学方程式如下:
2Al(OH)3+ 12HF+ 3Na2CO3=2Na3AlF6+3CO2↑+ 9H2O
根据题意完成下列填空:
(1)在上述反应的反应物和生成物中, 属于弱酸,电离方程式 。
(2)反应物中有两种元素在元素周期表中位置相邻,下列能判断它们的金属性或非金属性强弱的是 (选填编号)。
a.气态氢化物的稳定性 b.最高价氧化物对应水化物的酸性
c.单质与氢气反应的难易 d.单质与同浓度酸发生反应的快慢
(3)反应物中某些元素处于同一周期。它们最高价氧化物对应的水化物之间发生反应的离子方程式为 。
(4) Na2CO3俗称纯碱,属于 (填离子或共价)化合物。其中含有的化学键是 。
查看答案和解析>>
科目:高中化学 来源:2013届上海市高二上学期期中考试化学试卷 题型:填空题
工业上制取冰晶石(Na3AlF6)的化学方程式如下:
2Al(OH)3+ 12HF+ 3Na2CO3=2Na3AlF6+ 3CO2↑+ 9H2O
根据题意完成下列填空:
(1)在上述反应的反应物和生成物中,属于非极性分子的电子式 ,属于两性氢氧化物的电离方程式 。
(2)反应物中有两种元素在元素周期表中位置相邻,下列能判断它们的金属性或非金属性强弱的是 (选填编号)。
(A)、气态氢化物的稳定性 (B)、最高价氧化物对应水化物的酸性
(C)、单质与氢气反应的难易 (D)、单质与同浓度酸发生反应的快慢
(3)反应物中某些元素处于同一周期。它们最高价氧化物对应的水化物之间发生反应的离子方程式为 。
(4) Na2CO3俗称纯碱,属于 晶体。
查看答案和解析>>
科目:高中化学 来源:2010-2011年江苏省高一下学期期末考试化学试卷 题型:填空题
工业上制取冰晶石(Na3AlF6)的化学方程式如下,
2Al(OH)3+ 12HF+ 3Na2CO3=2Na3AlF6+ 3CO2↑+ 9H2O,根据题意完成下列填空:
(1)在上述反应的反应物和生成物中,属于非电解质的物质的电子式为 ,属于弱酸的电离方程式 。
(2)上述反应物中有两种元素在元素周期表中位置相邻,下列能判断它们的金属性或非金属性强弱的是 (选填编号)。
a.气态氢化物的稳定性 b.最高价氧化物对应水化物的酸性
c.单质与氢气反应的难易 d.单质与同浓度酸发生反应的快慢
(3)上述反应物中某些元素处于同一周期。它们最高价氧化物对应的水化物之间发生反应的离子方程式为 。
(4)上述产物当中有一个物质比同族元素类似化合物的沸点高很多,写出这个物质的结构式_______,其沸点较高的原因是_______________;反应物中属于盐的物质中含有的化学键有________________。(填“离子键”或“共价键”或“金属键”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com