
【题目】下列物质中属于电解质的是( )
A.NH3B.乙醇C.氯化钠D.氯水
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:
【题目】向0.1mol/L CH3COOH溶液中加入CH3COONa晶体或加水稀释时,都会引起
A. 溶液的pH增大 B. CH3COOH的电离程度增大
C. 溶液的导电能力减小 D. 溶液的c(OH-)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液经分析,其中只含有Na+、K+、Ca2+、Cl﹣、NO3﹣ , 已知其中K+、Ca2+、Na+、NO3﹣的浓度均为0.1mol/L,则Cl﹣ 物质的量浓度为( )
A.0.1 molL﹣1
B.0.3 molL﹣1
C.0.2 molL﹣1
D.0.4 molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 凡是能溶于水有甜味的物质都属于糖类 B. 糖类都能发生水解反应
C. 油脂、糖类都属于高分子化合物 D. 葡萄糖属于单糖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验能达到相应目的的是( )
选项 | A | B | C | D |
实验过程 |
|
|
|
|
实验目的 | 将乙二醇转化为乙二酸 | 比较氯化铁和二氧化锰对H2O2分解反应的催化效果 | 证明稀硝酸与铜反应时表现出氧化性 | 用SO2与Ba(NO3)2反应获得BaSO3沉淀 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温时CH3COOH的电离平衡常数Ka=1.75×105,NH3·H2O的电离平衡常数Kb=1.75×105。常温时,向10 mL浓度均为0.01mol·L1的NaOH和氨水混合溶液中,逐滴加入0.01mol·L1的 CH3COOH 溶液,混合溶液的pH与加入CH3COOH的体积V之间的变化曲线如图所示,下列有关说法正确的是

A. a 点溶液的pH<12
B. b 点时水的电离程度最大
C. c 点处的微粒间存在:c(CH3COO)=c(NH4+)+c(NH3·H2O)
D. d 点处的微粒间存在:c(CH3COO)>c(H+)>c(Na+)>c(NH4+)>c(OH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物M 有抗菌作用,其合成路线如下图所示:

已知:①![]()
②
③
(1)M的分子式是______________,A的化学名称是__________________。
(2)G的结构简式是___________,F中含氧官能团的名称是_______________。
(3)由A生成B和由G生成H 的反应类型分别是___________、____________。
(4)由C生成D 的化学方程式是_________________。
(5)E 的同分异构体中,符合下列条件的结构共有___________种。
①苯的二元取代物 ②与E 具有相同的官能团 ③能发生银镜反应和水解反应
(6)结合题给信息,以甲苯为原料制备化合物![]() ,设计合成路线(其他试剂任选)。 _________
,设计合成路线(其他试剂任选)。 _________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨和肼(N2H4)都是氮元素的重要氢化物,在工农业生产、生活中有广泛应用。
(1)工业中常用以下反应合成氨:N2+3H2![]() 2NH3 △H<0。某实验室在三个不同条件的密闭容器中,分别加入浓度均为c(N2)=0.100mol/L,c(H2)=0.300mol/L进行反应时,N2的浓度随时间的变化如下图①、②、③曲线所示:
2NH3 △H<0。某实验室在三个不同条件的密闭容器中,分别加入浓度均为c(N2)=0.100mol/L,c(H2)=0.300mol/L进行反应时,N2的浓度随时间的变化如下图①、②、③曲线所示:
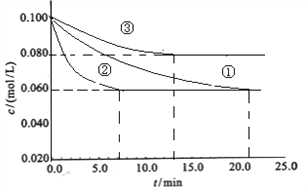
装罝③仅有一个反应条件与①不同,该条件为_______________,实验②平衡时H2的转化率为_____________;
(2)肼是一种具有强还原性的无色油状液体,可用作燃料。
①在火箭推进器中装有胼(N2H4)和液态H2O2,已知0.4mol液态N2H4和足量液态H2O2反应,生成气态N2和气态H2O,放出256.6kJ的热量。该反应的热化学方程式为_____________________________________________________。
②肼(N2H4)-空气燃料电池是一种环保型碱性燃料电池,电解质溶液是20%-30%的KOH溶液。已知肼在101kPa、25℃条件下的燃烧热为624kJ·mol-1,如果此燃料电池的能量转化率为50%,当消耗空气2.24L(已折算为标准状况下体积)时,则此电池产生的电能约为_________kJ。(假设空气中氧气的体积含量为20%,产物为液态水)

(3)肼又称“联氨”,为二元弱碱,在水中的电离方程式与氨相似,肼第一步电离反应的平衡常数值为____________.(已知:N2H4+H+![]() N2H5+ 的K=8.7×107;KW =1.0×10-14)
N2H5+ 的K=8.7×107;KW =1.0×10-14)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NaOH标准溶液滴定未知浓度的盐酸,用酚酞为指示剂,造成测定结果偏高的原因可能是
A. 配制标准溶液的NaOH中混有Na2CO3 杂质
B. 盛装待测液的锥形瓶用燕馏水洗过,没有用待测液洗
C. 滴定到终点读数时,俯视刻度线
D. 滴定到终点读数时,滴定管尖嘴处有气泡
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com