
| A���������� | B���ȼ�С��������ijֵ | C������ | D���������С��ijֵ |
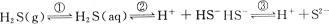



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��������Ӧ��ƽ�����ʣ�������� |
| B����Ӧ�����ʱ�䣺������� |
| C��������ʹ��ᷴӦ��п��������� |
| D����ʼʱ��Ӧ���ʣ�����=���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��c(H+)="c(HCl)" | B��c(H+)=c(HCl)+Kw/c(H+) |
| C��c(H+)=c(HCl)+Kw | D��c(H+)=c(HCl)?Kw/c(H+) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 H++HA-��HA-
H++HA-��HA- H++A2-�����ж�0.1 mol��L-1 H2A��Һ���й������������( )
H++A2-�����ж�0.1 mol��L-1 H2A��Һ���й������������( )�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
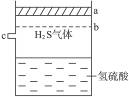
| A��a��b��c | B��a="b=c" | C��c��a��b | D��b��c��a |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| ���ữѧʽ | CH3COOH | HCN | H2CO3 |
| ����ƽ�ⳣ����25�棩 | 1.8��l0��5 | 4.9��l0��10 | K1=4.3��l0��7 K2=5.6��l0��11 |
| A�������ʵ���Ũ�ȵĸ���ҺpH��ϵΪ��pH��NaCN����pH��Na2CO3����pH��CH3COONa�� |
| B��a mol��L��1 HCN��Һ��b mol��L��1 NaOH��Һ�������Ϻ�������Һ��c(Na��)��c(CN��)����aһ������b |
| C������������μ�ˮ������Һ�ĵ����ԡ�����ĵ���ȡ�pH����������С |
| D��NaHCO3��Na2CO3�����Һ�У�һ������c(Na��)+ c(H��)=c(OH��)+ c(HCO3��) +2c(CO32��) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��CH3COOH�� | B��H2SO4 | C��NaOH | D��Na2CO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A��H2S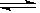 2H++S2�� 2H++S2�� | B��Al��OH��3==Al3+ + 3OH- |
C��NH3��H2O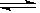 NH4+ +OH�� NH4+ +OH�� | D��NaHCO3 ==Na++ H+ + CO32�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���������� | B������ | C������ | D���Ȼ��� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com