
��12�֣�ijС��ͬѧ���Ʊ�������ͭʱ����20 mL 2 mol/L��NaOH��Һ����50 mL 1 mol/L��CuSO4��Һ�У��õ�����ɫ����.���롰������ͭ����ɫ��������һ����˵��������Ϊ̽������ɫ�����ijɷ֣�������������ʵ�����̽��. ��
[ʵ��һ]
��20 mL 1 mol/L��CuSO4��Һ����50 mL 2 mol/L��NaOH��Һ�У��۲쵽��������ɫ����.
[ʵ���]
�ٽ���ɫ�������ˡ�ϴ�ӡ����º��.
�ڳ�ȡ2.58 g����ɫ������Ͷ��50 mL 2 mol/L��NaOH��Һ�У����������������ɫ�����ˡ�ϴ�ӣ�����ϴ��Һת�Ƶ���Һ�У����º�ɳ�������ɫ����Ϊ1.96 g.
����ڵ���Һ�м��������Ȼ�����Һ���а�ɫ�������ɣ����ˡ�ϴ�ӡ���ɺ����Ϊ2.33 g.
��ش��������⣺
��1������220ml 1mol/L������ͭ��Һ������������ƽ��ҩ�ס��ձ�������������Ͳ����ͷ�ι��⣬����Ҫ�IJ��������� ����ʵ������������� ��
��2������ͬѧ��ʵ��һ��Ŀ�Ļ�������
��3��ʵ����еڢٲ�ϴ�ӳ����ķ����ǡ�
��4��ͨ�����㣬����ɫ�����ijɷֿɱ�ʾΪ�� .
��5��д��ʵ����еڢڲ�������Ӧ�����ӷ���ʽ��
��1�� 250ml����ƿ 62.5
��2��������ʵ�飬ȷ����ɫ��������������ͭ(��ȷ����ɫ��������ɫ��������ͬһ������)
��3����������м�ˮ���պý�û����Ϊֹ����ˮ��Ȼ������ظ�����2~3�Ρ�
��4�� Cu2(OH)2SO4��Cu(OH)2��CuSO4
��5��Cu(OH)2��CuSO4��2OH����2Cu(OH)2��SO42��(��Cu2(OH)2SO4��2OH����2Cu(OH)2��SO42��)��
��������
�����������1������220ml 1mol/L������ͭ��Һ������������ƽ��ҩ�ס��ձ�������������Ͳ����ͷ�ι��⣬����Ҫ�IJ���������250ml����ƿ����ʵ�������������������Ӧ�ð���250ml��Һ�����㣬m(����)= 0.25L��1mol/L��250g/mol=62.5g����2������ͬѧ��ʵ��һ��Ŀ�Ļ�������������ʵ�飬��ȷ����ɫ��������������ͭ(��ȷ����ɫ��������ɫ��������ͬһ������) ����3��ʵ����еڢٲ�ϴ�ӳ����ķ�������������м�ˮ���պý�û����Ϊֹ����ˮ��Ȼ������ظ�����2~3�Σ���4����ȡ2.58 g����ɫ�����к��У�n(SO42��)= 2.33 g��233g/mol=0.01mol��n(Cu2+)=1.96 g��98g/mol=0.02mol,����n(OH��)= (2.58 g��0.01mol��96g/mol-0.02mol��64g/mol)��17g/mol=0.02mol, n(Cu2+)��n(OH��)��n(SO42��)= 0.02:0.02:0.01=2:2:1�����Ը���ɫ�����ijɷֿɱ�ʾΪCu2(OH)2SO4��Cu(OH)2��CuSO4 ����5����ʵ����еڢڲ�������Ӧ�����ӷ���ʽ��Cu(OH)2��CuSO4��2OH����2Cu(OH)2��SO42������Cu2(OH)2SO4��2OH����2Cu(OH)2��SO42������
���㣺�������ʵ���Ũ�ȵ���Һ���Ƶ�������ʹ�á�������ϴ�ӷ��������ʻ�ѧʽ��ȷ����֪ʶ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ�����ڶ����¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪A��B��C��D֮���ת����ϵΪ��A + B �� C + D���������й�˵������ȷ����
A����AΪFe��DΪ��������B�������ᣬҲ������ˮ
B����A��DΪ�����BΪˮ����C���������嵥�ʣ�Ҳ�����ǻ�����
C����A��B��C��D��Ϊ������÷�Ӧһ�����ڸ��ֽⷴӦ
D����A��B��C��D��Ϊ10����������C�ǿ�ʹʪ��ĺ�ɫʯ����ֽ���������壬��D �ڳ�����һ����Һ̬
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ������ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��������ʵ�鷽�����ԴӺ��������������ȡ���п��������õĻ������ʡ�����˵���������
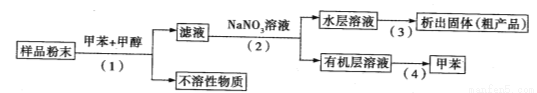
A�����裨1����Ҫ����װ�� B�����������������л��ܼ���������ˮ
C�����裨3����Ҫ�õ������� D�����裨4�����������ʵķе������з����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ������ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
ˮ�ȷ��Ʊ�ֱ��Ϊ1~100 nm�Ŀ���Y�����������Ӧԭ��Ϊ��
3Fe2+ + 2S2O32- + O2 + aOH��= Y+ S4O62- + 2H2O������˵���в���ȷ����
A��a��4
B����Y���ȷ�ɢ��ˮ���γɵ���ϵ���ж����ЧӦ
C��ÿ��3 mol Fe2+ �μӷ�Ӧ����Ӧ��ת�Ƶĵ�������Ϊ5 mol
D��S2O32-�ǻ�ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ������ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����ж���һ����ȷ����:
A�������ʵ�����CaCl2��CaO2������������������֮�Ⱦ�Ϊ2��1
B����������O2��O3�У���ԭ�ӵĸ�����Ϊ3��2
C���ֱ���H2O2��KMnO4�ֽ���O2�����Ƶõ�����O2ʱ��ת�Ƶ�����֮��Ϊ1��2
D��10mL 0��3mol��L��1NaCl��30mL0��1mol��L��1AlCl3��Һ��Cl�����ʵ���Ũ�ȱ�Ϊ1��3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ������һ��ģ�⿼�Ի�ѧ�Ծ��������棩 ���ͣ������
ij��Һ�п��ܺ�������6�������еļ��֣�NH4+��A13+��Mg2+��CO32�D��Clһ��SO42�D��Ϊȷ����Һ����ɣ���ȡ100 mL�ֳ����ȷ���Һ��������ʵ�飺
��1�����һ����Һ�м��� AgNO3��Һ�г���������
��2����ڶ�����Һ�м�������NaOH��Һ��ַ�Ӧ�����յõ�����0.58 g��ͬʱ�ռ�������0.03 mol(������ȫ������Һ���ݳ�)��
��3�����������Һ�м�������BaCl2��Һ(�����ữ)��ַ�Ӧ�õ�����6.99 g��
�ɴ˿�֪�����й���ԭ��Һ��ɵ���ȷ�����ǣ� ��
A����Һ��SO42�D��Ũ����0. 3 mol/L B����Һ��һ������A13+��NH4+
C��һ��������Mg2+�����ܴ���A13+ D��һ������Clһ ���ܺ�CO32��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ������һ��ģ�⿼�Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��KClO3��I2��0.02 mol����12 ��36.5���������У�I2ǡ����ȫ�ܽ⣬û���������(����������Ļӷ�)������Ӧ�����Һ�ñ�ˮ��ȴ�������Ⱥ�ɫ����A(A�ڳ����¾�����������)�����ˣ�����Һ���ɣ��ռ���KCl���塢8.7gҺ̬ˮ�ͼ�������A��������A�Ļ�ѧʽ�����ǣ� ��
A��I2Cl6 B��ICl5 C��HClO D�� KIO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��[ͬ��]2015���ʱ����³�ư����2����ʱ6Ԫ�����ڱ���Ԫ�������ɣ������棩 ���ͣ�ѡ����
�������ж�����Ԫ�����ʵ����ݣ�
Ԫ�ر��
Ԫ������ | �� | �� | �� | �� | �� | �� | �� | �� |
ԭ�Ӱ뾶 | 0��74 | 1��60 | 1��52 | 1��10 | 0��99 | 1��86 | 0��75 | 0��82 |
����ϼ� |
| ��2 | ��1 | ��5 | ��7 | ��1 | ��5 | ��3 |
��ͻ��ϼ� | ��2 |
|
| ��3 | ��1 |
| ��3 |
|
����˵����ȷ����( )
A��Ԫ��ԭ�������ܴ��ڢ�
B���ڡ��ۺ�Ԫ�ش���ͬһ����
C���ݺ�Ԫ������������ˮ����������ǿ
D�����Ԫ���ǽ���Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��[ͬ��]2015��ͬ����ʱ���˽�ѡ��5��2-1������ϩ�� ϩ��˳���칹�������棩 ���ͣ�ѡ����
�������ʷе������˳����ȷ����( )
�ٶ��� ��2?������ ������ ��2?������ ��2,2?��������
A���٣��ڣ��ۣ��ܣ���
B���ݣ��ܣ��ۣ��ڣ���
C���ۣ��ܣ��ݣ��٣���
D���ڣ��٣��ݣ��ܣ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com