
有X、Y两种元素,原子序数≤20,X的原子半径小于Y,且X、Y原子的最外层电子数相同(选项中m、n均为正整数)。下列说法正确的是
A.若X(OH)n为强碱,则Y(OH)n也一定为强碱
B.若HnXOm为强酸,则X的氢化物溶于水一定显酸性
C.若X元素为非金属元素,则Y元素也一定为非金属元素
D.若Y的最高正价为+m,则X的最高正价一定为+m
 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:
能正确表示下列反应的离子方程式是 ( )
A.用过量氨水吸收工业尾气中的SO2:2NH3·H2O+SO2===2NH +SO
+SO +H2O
+H2O
B.氯化钠与浓硫酸混合加热:H2SO4+2Cl-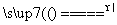 SO2↑+Cl2
SO2↑+Cl2 ↑+H2O
↑+H2O
C.磁性氧化铁溶于稀硝酸:3Fe2++4H++NO ===3Fe3++NO↑+3H2O
===3Fe3++NO↑+3H2O
D.明矾溶液中滴入Ba(OH)2溶液使SO 恰好完全沉淀:2Ba2++3OH-+Al3++2SO
恰好完全沉淀:2Ba2++3OH-+Al3++2SO ===2BaSO4↓+Al(OH)3↓
===2BaSO4↓+Al(OH)3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
研究有机物的方法有很多,常用的有①核磁共振氢谱②蒸馏③重结晶④萃取⑤红外光谱⑥过滤,其中用于有机物分离或提纯的方法有_____________,用于分子结构确定的有 __________。(填序号)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关127 53I和131 53I说法,正确的是
A.127 53I和131 53I的核外电子数不同 B.127 53I和131 53I的中子数分别为74和78
C.127 53I和131 53I属不同种元素 D.127 53I和131 53I是同一种核素
查看答案和解析>>
科目:高中化学 来源: 题型:
对反应 4NH3 + 5O2 = 4NO + 6H2O,下列反应速率的最快的是
A. v(NH3)=0.25 mol·L-1·min-1 B. v(O2)=0.35mol·L-1·min-1
C. v(NO)=0.01 mol·L-1·S-1 D. v(H2O)=0.3 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
在300℃、70MPa下由二氧化碳和氢气合成乙醇已成为现实。
2CO2(g) + 6H2(g) CH3CH2OH(g) + 3H2O(g) 下列叙述错误的是
CH3CH2OH(g) + 3H2O(g) 下列叙述错误的是
A.使用Cu-Zn-Fe催化剂可大大提高CH3CH2OH的产率
B.反应需在300℃进行可推测出该反应为吸热反应
C.充入大量CO2气体可提高H2的转化率
D.从平衡混合气体中分离出CH3CH2OH和H2O可提高CO2和H2的利用率
查看答案和解析>>
科目:高中化学 来源: 题型:
硫代硫酸钠溶液与稀硫酸的反应方程式为:
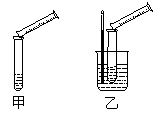 Na2S2O3+H2SO4 = Na2SO4+S↓+SO2+H2O,某实验兴趣小组用如下图所示的实验装置探究外界条件对化学反应速率的影响(加热仪器和夹持仪器均已省略)。
Na2S2O3+H2SO4 = Na2SO4+S↓+SO2+H2O,某实验兴趣小组用如下图所示的实验装置探究外界条件对化学反应速率的影响(加热仪器和夹持仪器均已省略)。
(1)实验目的:装置甲,探究浓度对化学反应速率的影响;装置乙,探究 对化学反应速率的影响。
(2)通过甲、乙装置,分别进行了三组实验,数据记录如下,并经分析得出相关结论:
| 实验 组号 | 温度 | Na2S2O3溶液 | H2SO4 | 加入H2O的体积 | 出现沉淀所需时间 | ||
| 体积 | 浓度 | 体积 | 浓度 | ||||
| Ⅰ | 0℃ | 5mL | 0.1mol·L—1 | 10mL | 0.1mol·L—1 | 5mL | 8s |
| Ⅱ | 0℃ | 5mL | 0.1mol·L—1 | 5mL | 0.1mol·L—1 | 10mL | 12s |
| Ⅲ | 30℃ | 5mL | 0.1mol·L—1 | 5mL | 0.1mol·L—1 | 10mL | 4s |
结论1:由Ⅰ和Ⅱ两组数据可知 ;
结论2:由Ⅱ和Ⅲ两组数据可知 。
查看答案和解析>>
科目:高中化学 来源: 题型:
有a、b、c、d四个金属电极,有关的反应装置及部分反应现象如下:
| 实验 装置 |
|
|
|
|
| 部分实验现象 | a极质量减小b极质量增加 | c极有气体产生 b极质量减轻 | d极溶解c极有气体产生 | 电流从a极流向d极 |
由此可判断这四种金属的活动性顺序是( )
A. a>b>c>d B. b>c>d>a
C. d>a>b>c D. a>b>d>c
查看答案和解析>>
科目:高中化学 来源: 题型:
有两种饱和一元醇, 它们分子中的碳原子个数相差1, 已知它们的某种混合物8g与足量金属钠反应后可生成2.24L(标准状况)氢气, 则它们分别是
A.甲醇、乙醇 B. 甲醇、丙醇 C.丙醇、丁醇 D.丁醇、戊醇
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com