
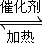 2SO3(g),SO2的转化率随温度的变化如下表所示:
2SO3(g),SO2的转化率随温度的变化如下表所示:| 温度°C | 450 | 500 | 550 | 600 |
| SO2的转化率% | 97.5 | 95.8 | 90.50 | 80.0 |
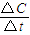 计算v(O2);
计算v(O2); =0.16mol?L-1,故v(O2)=
=0.16mol?L-1,故v(O2)=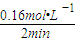 =0.08mol/(L?min),故答案为:0.08mol?L-1?min-1;
=0.08mol/(L?min),故答案为:0.08mol?L-1?min-1;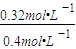 ×100%=80%,所以此时的温度为600℃,故答案为:600;
×100%=80%,所以此时的温度为600℃,故答案为:600;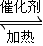 2SO3(g),
2SO3(g),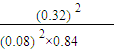 =
=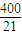 ,
,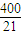 ;
;

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 催化剂 |
压强 SO2的 转化率 温度 |
1×105 Pa | 5×105 Pa | 10×105 Pa | 50×105 Pa | 100×105 Pa |
| 450℃ | 97.5% | 98.9% | 99.2% | 99.6% | 99.7% |
| 550℃ | 85.6% | 92.9% | 94.9% | 97.7% | 98.3% |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
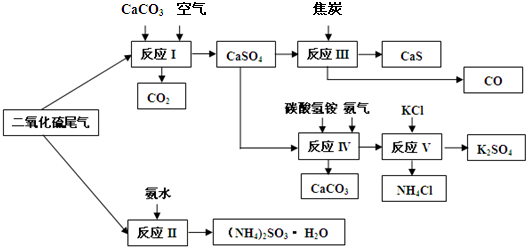
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com