
| A.0.5 mol苯分子中含有C=C双键数为1.5NA |
| B.1 mol甲基(—CH3)所含的电子总数为10NA |
C.标准状况下,1L甲醇完全燃烧后生成的CO2分子数目约为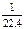 NA NA |
| D.2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案科目:高中化学 来源:不详 题型:单选题

| A.60gSiO2晶体中含有2×6.02×1023个Si—O键 |
| B.18gD2O(重水)完全电解,转移2×6.02×1023个电子 |
| C.720gC60晶体(如右图)中含有6.02×1023个晶胞结构单元 |
| D.14g两种烯烃CnH2n和CmH2m混合物,含有共用电子对数目为3×6.02×1023 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.X2气体过量 | B.X2和Y2的体积均为50ml |
| C.产物是气态双原子分子 | D.无法判断 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 表示阿伏加德罗常数,下列叙述中正确的是( )
表示阿伏加德罗常数,下列叙述中正确的是( )A.常温常压下,11.2L氧气所含有的电子数为 |
B.1.8g的 离子中含有的电子数为 离子中含有的电子数为 |
C.常温常压下,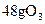 含有的氧原子数为 含有的氧原子数为 |
D.2.4g金属镁变为镁原子时失去的电子数为 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1mol某气体的体积为22.4L,该气体的状况不一定是标准状况 |
| B.在非标准状况下,1mol气体的体积一定不是22.4L |
| C.某物质含有阿伏加德罗常数个微粒,它在标准状况下的体积一定为22.4L |
| D.在标准状况下,1molO2和N2的混合气体的体积不一定是约22.4L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.53g碳酸钠晶体中含0.5NA个CO32-离子 |
| B.标准状况下的22.4L辛烷完全燃烧,生成二氧化碳分子数为8NA |
| C.1molOH-放电被氧化时失去NA的电子 |
| D.在2.8g晶体硅中含有0.2NA个Si-Si键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 NA表示阿伏加德罗常数,下列说法正确的是( )
NA表示阿伏加德罗常数,下列说法正确的是( )| A.1molOH-含有电子数为8NA |
| B.在标准状况下,22.4L氯气含有原子数为NA |
| C.在常温常压下,1mol氩气所含原子数为2NA |
| D.32g铜和足量硫完全反应,生成Cu2S,转移的电子数为0.5 NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com