
超细氮化铝粉末被广泛应用于大规模集成电路生产等领域,其制取原理为Al2O3+N2+3C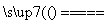 2AlN+3CO,由于反应不完全,氮化铝产品中往往含有炭和氧化铝杂质,为测定该产品中有关成分的含量,进行了以下两个实验。
2AlN+3CO,由于反应不完全,氮化铝产品中往往含有炭和氧化铝杂质,为测定该产品中有关成分的含量,进行了以下两个实验。
(1)称取10.00 g产品,将其加入过量的NaOH浓溶液中共热并蒸干,AlN跟NaOH溶液反应生成Na[Al(OH)4],并放出氨气3.36 L(标准状况)。
①上述反应的化学方程式为______________________________________________;
②计算该样品中AlN的质量分数。
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
(2)另取10.00 g样品置于反应器中,通入2.016 L(标准状况)O2,在高温下充分反应后测得气体的密度为1.34 g·L-1(已折算成标准状况,AlN不跟O2反应)。计算该样品中含杂质炭的质量。
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
科目:高中化学 来源: 题型:
下列关于碳纤维增强树脂基复合材料的说法正确的是( )
A.碳纤维复合材料的基体是碳纤维
B.碳纤维复合材料的增强体是合成树脂
C.碳纤维复合材料具有韧性好、强度大、质脆质轻的特点
D.碳纤维复合材料具有可燃性
查看答案和解析>>
科目:高中化学 来源: 题型:
二氧化硅属于酸性氧化物的理由主要是( )
A.硅是非金属元素
B.二氧化硅能与NaOH溶液反应生成盐和水
C.二氧化硅不能与酸(除HF外)反应
D.高温下,二氧化硅能与Na2CO3反应生成二氧化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:Fe2O3+3CO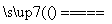 2Fe+3CO2。
2Fe+3CO2。
(1)标出该反应中电子转移的方向和数目。
________________________________________________________________________
(2)该反应中____元素被还原,____元素被氧化。
(3)在该反应中,若有2 mol电子发生转移,在标准状况下,可生成CO2的体积为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
向Fe和Fe2O3的混合物中加入足量的稀硫酸,充分反应后生成FeSO4溶液,当生成的Fe2+和H2的物质的量之比为5︰2时,则Fe和Fe2O3的物质的量之比为 ( )
A.3︰1 B.1︰2 C.2︰1 D.1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A为ⅡA族元素,B为ⅢA族元素,它们的原子序数分别为m和n,且A、B为同一周期元素,下列错误的是( )
A.n=m+1 B.n=m+11
C.n=m+25 D.n=m+10
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com