
【题目】0.2 mol 某烃 A在氧气中完全燃烧后,生成 CO2 和 H2O 各 1.2 mol。试回答:
(1)烃 A 的分子式为_____。
(2)若烃A不能使溴水褪色,但在一定条件下能与氯气发生取代反应,其一氯取代物只有一种,则烃A 的键线式为_____。
(3)若烃A能使溴水褪色,在催化剂作用下,与H2 加成,其加成产物经测定分子中含有4个甲基,烃A可能有的结构简式为 _______。(任写一种即可)
(4)比烃 A 少一个碳原子且能使溴水褪色的 A 的同系物有____种同分异构体。
【答案】C6H12 ![]() (CH3)3CCH=CCH2 5
(CH3)3CCH=CCH2 5
【解析】
(1)烃燃烧生成二氧化碳和水,由0.2mol烃燃烧生成二氧化碳和水各1.2mol计算可得分子式;
(2)若烃A不能使溴水褪色,但在一定条件下,能与Cl2发生取代反应,其一氯代物只有一种,说明烃中不含碳碳双键;
(3)烃A能使溴水褪色,在催化剂作用下,与H2加成,其加成产物经测定分子中含有4个甲基,说明烃中含有C=C,其中,含有4个甲基的有3种,其碳架结构为(①②③处可分别不同时安排双键):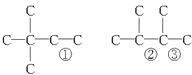 ,以此确定烯烃;
,以此确定烯烃;
(4)比烃A少一个碳原子且能使溴水褪色的A的同系物,分子式为C5H10,含有1个C=C双键,据此书写符合条件的同分异构体判断。
(1)某烃A0.2mol在氧气中完全燃烧后,生成CO2和H2O各1.2mol,则分子中含有N(C)=6,N(H)=12,分子式为C6H12;
(2)C6H12只有1个不饱和度,若烃A不能使溴水褪色,则其为环烷烃。其中,能与氯气发生取代反应,其一氯代物只有一种的是环己烷,即![]() ;
;
(3)烃A能使溴水褪色,在催化剂作用下,与H2加成,其加成产物经测定分子中含有4个甲基,说明烃中含有C=C,其中,含有4个甲基的有3种,其碳架结构为(①②③处可分别不同时安排双键): ,烃A可能有的结构简式为(CH3)3CCH=CH2、CH3C(CH3)=C(CH3)CH3、CH3CH(CH3)C(CH3)=CH2等;
,烃A可能有的结构简式为(CH3)3CCH=CH2、CH3C(CH3)=C(CH3)CH3、CH3CH(CH3)C(CH3)=CH2等;
(4)比烃A少一个碳原子且能使溴水褪色的A的同系物,分子式为C5H10,含有1个C=C双键,符合条件的同分异构体为:CH3CH2CH2CH=CH2,CH3CH2CH=CHCH3,CH2=C(CH3)CH2CH3,(CH3)2C=CHCH3,(CH3)2CHCH=CH2,共5种。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】有下列几组物质,请将序号填入下列空格内:
A、CH2=CH﹣COOH和油酸( C17H33COOH)
B、12C60和石墨
C.![]() 和
和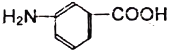
D.35Cl和37Cl
E.乙醇和乙二醇
(1)互为同位素的是_____。
(2)互为同系物的是_____。
(3)互为同素异形体的是:_____。
(4)互为同分异构体的是_____。
(5)既不是同系物,又不是同分异体,也不是同素异形体,但可看成是同一类物质的是_____
(6)写出乙醇的催化氧化方程式:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一个实验室制取氯气并以氯气为原料进行特定反应的装置:
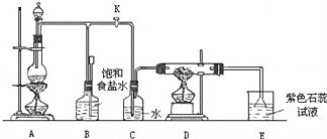
(1)A是氯气发生装置,其中反应的化学方程式为_____。
(2)实验开始时,先点燃A处的酒精灯,打开旋塞K,让Cl2充满整个装置,再点燃D处酒精灯,连接上E装置。Cl2通过C瓶后再进入D。D装置的硬质玻璃管内盛有炭粉,发生氧化还原反应,其产物为CO2和HCl。试写出D中反应的化学方程式:_____。装置C的作用是_____。
(3)在E处,紫色石蕊试液的颜色由紫色变为红色,再变为无色,其原因是_____。
(4)若将E处烧杯中溶液改为澄清石灰水,反应过程现象为_____(选填标号)。
A.有白色沉淀生成 B.无现象 C.先生成白色沉淀,而后白色沉淀消失
(5)D处反应完毕后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有Cl2产生,此时B中的现象是_____,B的作用是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知KMnO4与浓HCl在常温下反应能产生Cl2。若用下图所示的实验装置来制备纯净、干燥的氯气,并试验它与金属的反应。每个虚线框表示一个单元装置,其中错误的是( )

A.只有①和②处B.只有②处C.只有②和③处D.只有②③④处
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胡妥油(D)是香料的原料,它可由 A 合成得到: 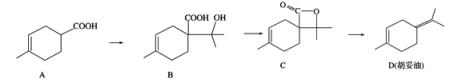
下列说法正确的是( )
A.有机物 B 的分子式为 C11H19O3
B.1mol B 与足量的 Na 反应可产生 11.2LH 2 (已换算成标准状况)
C.有机物 C 的所有同分异构体中可能有芳香族化合物存在
D.一定条件下,A分别可以发生加成、取代、氧化等反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的转化在给定条件下能实现的是( )
A.Fe3O4(s) ![]() Fe(s)
Fe(s) ![]() Fe(NO3)3(aq)
Fe(NO3)3(aq)
B.Al2O3 ![]() AlCl3(aq)
AlCl3(aq) ![]() 无水AlCl3
无水AlCl3
C.Fe2O3(s) ![]() Fe(s)
Fe(s) ![]() FeCl3(aq)
FeCl3(aq)
D.CuSO4(aq) ![]() Cu(OH)2
Cu(OH)2![]() CuO
CuO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以高硫铝土矿(主要成分为Al2O3、Fe2O3、SiO2,少量FeS2和金属硫酸盐)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如下:
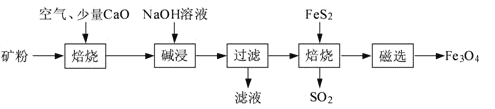
(1)粉碎高硫铝土矿石的目的是______。
(2)焙烧时发生氧化还原反应:______FeS2+______O2![]() ______Fe2O3+______SO2↑,配平该方程式。
______Fe2O3+______SO2↑,配平该方程式。
(3)碱浸时发生反应的化学方程式为______。
(4)过滤后向滤液中通入过量的CO2气体,反应的离子方程式为______。
(5)“过滤”得到的滤渣中含有大量的Fe2O3。Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,理论上完全反应消耗的n(FeS2):n(Fe2O3)=______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定量的Fe、FeO、Fe3O4的混合物中加入100mL2mol/L的盐酸,恰好使混合物完全溶解,放出224mL(标准状况)的气体,所得溶液中加入KSCN溶液无血红色出现。若用足量的CO在高温下还原相同质量的此混合物,能得到铁的质量是( )
A. 11.2gB. 5.6gC. 2.8gD. 无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)如图为测定中和热的实验装置图。请回答下列问题:
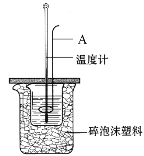
①仪器A的名称为___;
②如果用0.50mol·L-1的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”的数值将___(填“偏大”、“偏小”或“不变”)
(2)近期发现,H2S是继NO、CO之后的第三个生命体系气体信号分子,它具有参与调节神经信号传递、舒张血管减轻高血压的功能。如图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。

①根据如图,请写出系统(II)中制氢的热化学方程式___;
②系统(I)和系统(II)相比,制得等量H2所需能量较少的是__(填“I”或“II”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com