
| A.用食醋清洗热水瓶中的水垢 |
| B.用米汤检验碘盐中含有碘酸钾 |
| C.用纯碱溶液洗涤餐具上的油污 |
| D.用丁达尔效应区别鸡蛋自溶液和食盐水 |
科目:高中化学 来源:不详 题型:单选题
| A.金属元素与非金属元素能形成共价化合物 |
| B.只有在原子中,质子数才与核外电子数相等 |
| C.完全由非金属元素形成的化合物中不含离子键 |
| D.非金属元素形成的共价化合物中,原子的最外层电子数只能是2或8 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.冰熔化时,分子中H—O键发生断裂 |
| B.原子晶体中,共价键的键长越短,键能越大,熔点就越高 |
| C.分子晶体中,共价键键能越大,该分子的熔沸点就越高 |
| D.分子晶体中,分子间作用力越大,则分子越稳定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 代号 | 物质 | 结构简式 | 水中溶解度/g (25℃) | 熔点/℃ | 沸点/℃ |
| A | 对—硝基苯酚 | 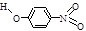 | 1.7 | 114 | 295 |
| B | 邻—硝基苯酚 | 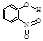 | 0.2 | 45 | 100 |
| | 熔点/K | 沸点/K | 标准状况时在水中的溶解度 |
| 甲 | 187 | 202 | 2.6 |
| 乙 | 272 | 423 | 以任意比互溶 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.配合物中中心原子的电荷数和配位数均为6 |
| B.该配合物可能是平面正方形结构 |
| C.Cl-和NH3分子均与Pt4+配位 |
| D.配合物中Cl-与Pt4+配位,而NH3分子与Pt4+不配位 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.含氢元素的化合物中一定有氢键 |
B.因为氢键的缘故,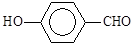 比 比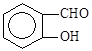 熔沸点高 熔沸点高 |
| C.由于氢键比范德华力强,所以H2O分子比H2S分子稳定 |
| D.“可燃冰”——甲烷水合物(例如:8CH4·46H2O)中CH4与H2O之间存在氢键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.胶体区别于其他分散系的本质特征是分散质微粒直径在1 nm~100 nm之间 |
| B.NH3的沸点高于PH3,是因为N-H键能大于P-H键能 |
| C.金属阳离子只存在于离子晶体中 |
| D.由非金属元素组成的化合物一定是共价化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com