
| A. | 若电解质溶液为KOH溶液,则电池工作一段时间后pH有明显变化 | |
| B. | Zn作负极,被氧化 | |
| C. | Ag2O在正极上发生还原反应 | |
| D. | 电解质溶液中的阴离子移向负极 |
分析 根据电池反应式知,Zn失电子作负极,Ag2O作正极,负极反应式为Zn+2OH--2e-═ZnO+H2O、正极反应式为Ag2O+H2O+2e-═2Ag+2OH-,放电时,电解质溶液中阴离子向负极移动、阳离子向正极移动,据此分析解答.
解答 解:A.根据电池反应式知,KOH不参加反应,也没有其它溶质或溶剂生成,所以理论上该电池工作一段时间后,溶液中KOH的浓度不变,pH没有明显变化,故A错误;
B.该反应中Zn元素化合价由0价变为+2价,所以Zn失电子作负极,被氧化,故B正确;
C.该反应中Ag元素化合价由+1价变为0价,Ag2O作正极,发生还原反应,故C正确;
D.放电时,电解质溶液中阴离子向负极移动,阳离子向正极移动,故D正确;
故选A.
点评 本题考查化学电源新型电池,为高频考点,正确判断正负极是解本题关键,难点是电极反应式的书写,易错选项是D,知道阴阳离子移动方向,题目难度不大.


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:选择题
| A. | 1.2mol/L | B. | 1.4mol/L | C. | 1.7mol/L | D. | 1.9mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
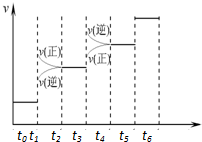 已知N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ•mol-1.请回答:(1)当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如右图所示.图中tl时引起平衡移动的条件可能是增大压强.其中表示平衡混合物中NH3的含量最高的一段时是t2-t3.
已知N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ•mol-1.请回答:(1)当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如右图所示.图中tl时引起平衡移动的条件可能是增大压强.其中表示平衡混合物中NH3的含量最高的一段时是t2-t3.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
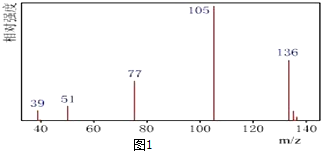
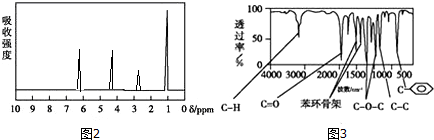
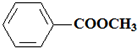 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 在锌与盐酸反应的实验中,某同学得到的结果如下表所示:
在锌与盐酸反应的实验中,某同学得到的结果如下表所示:| 锌的质量/g | 锌的形状 | 温度/℃ | 锌完全溶解的时间/s | |
| A | 2 | 薄片 | 5 | 400 |
| B | 2 | 薄片 | 15 | 200 |
| C | 2 | 薄片 | 25 | 100 |
| D | 2 | 薄片 | 35 | t1 |
| E | 2 | 颗粒 | 15 | t2 |
| F | 2 | 粉末 | 15 | t3 |
| G | 2 | 薄片(含少量杂质Cu) | 35 | t4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它们都含有 92个中子 | B. | 235U原子核外有143个电子 | ||
| C. | 它们互为同位素 | D. | 它们是同种核素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为保证分液漏斗内的液体顺利流出,需将上面的塞子拿下 | |
| B. | 进行分液时,分液漏斗中的下层液体从下端流出,上层则从上口倒出 | |
| C. | 萃取、分液前需对分液漏斗进行检漏 | |
| D. | 选用酒精萃取碘水中的碘单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 全部正确 | B. | ⑦⑧ | C. | ①③⑤⑥⑦ | D. | ①③⑦⑧ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com