
| A. | 使用催化剂,可加快反应速率,目的是提高生产效率 | |
| B. | 使用冰箱保存食物,是利用了化学反应速率理论 | |
| C. | 化学反应速率理论是研究怎样提高原料转化率 | |
| D. | 化学平衡理论是研究怎样使用有限原料多出产品 |
分析 在工业生产中,结合影响化学反应速率的因素可调节外界条件,加快产品的生成速率,从影响化学平衡的因素的角度选择合适的反应条件,使反应向生成物的方向进行,以此解答该题.
解答 解:A.使用催化剂,加快反应速率,缩短达到化学平衡的时间,可提高生产效率,故A正确;
B.降低温度,化学反应速率降低,利用了化学反应速率理论,故B正确;
C.化学平衡理论是研究怎样提高原料转化率,化学反应速率与转化率无关,故C错误;
D.促进化学平衡的向右移动,可生产较多的产品,利用了化学平衡理论,故D正确.
故选C.
点评 本题考查化学反应速率以及化学平衡的调控在工业生产中的应用,为高频考点,侧重于学生的分析能力的考查,有利于培养学生良好的科学素养,题目难度不大,注意工业生产所选择的反应条件应有利于转化率和产率的提高.


科目:高中化学 来源: 题型:选择题
| A. | 由水电离产生的c(H+)=10-12 mol•L一1的溶液中:K+、Na+、Fe2+、NO3- | |
| B. | 常温下,pH=7的溶液中:Al3+、Cl-、HCO3-、SO42- | |
| C. | 常温下,$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-12的溶液:K+、Cu2+、S2-、Cl- | |
| D. | pH=1的溶液中:Fe3+、NO3-、SO42-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
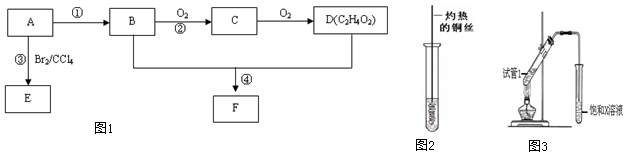
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 摩尔质量为17 g•mol-1 | |
| B. | 所含的分子数目约为9.03×1023 | |
| C. | 在标准状况下体积约为33.6L | |
| D. | 溶于水制成0.5L溶液时物质的量浓度为1.5mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 成分 | 质量(g) | 摩尔质量(g•mol-1) |
| 蔗糖 | 25.00 | 342 |
| 硫酸钾 | 0.87 | 174 |
| 阿司匹林 | 0.17 | 180 |
| 高锰酸钾 | 0.316 | 158 |
| 硝酸银 | 0.075 | 170 |
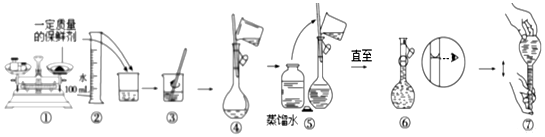
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
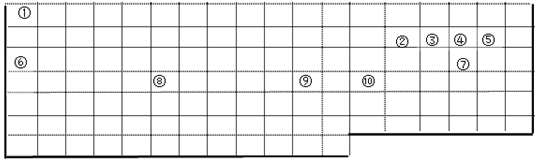

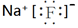 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com