(2011?四川)开发氢能是实现社会可持续发展的需要.硫铁矿(FeS
2)燃烧产生的SO
2通过下列碘循环工艺过程既能制H
2SO
4,又能制H
2.
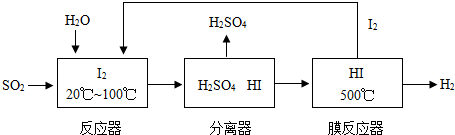
请回答下列问题:
(1)已知1g FeS
2完全燃烧放出7.1kJ热量,FeS
2燃烧反应的热化学方程式为
4FeS2(s)+11O2(g)=2Fe2O3(s)+8SO2(g)△H=-3408kJ?mol-1
4FeS2(s)+11O2(g)=2Fe2O3(s)+8SO2(g)△H=-3408kJ?mol-1
.
(2)该循环工艺过程的总反应方程式为
SO2+2H2O=H2SO4+H2
SO2+2H2O=H2SO4+H2
.
(3)用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H
2的目的是
有利于平衡向右移动,有利于碘和氢气的生成
有利于平衡向右移动,有利于碘和氢气的生成
.
(4)用吸收H
2后的稀土储氢合金作为电池负极材料(用MH)表示),NiO(OH)作为电池正极材料,KOH溶液作为电解质溶液,可制得高容量,长寿命的镍氢电池.电池充放电时的总反应为:NiO(OH)+MH
Ni(OH)
2+M
①电池放电时,负极的电极反应式为
MH-e-+OH-=H2O+M
MH-e-+OH-=H2O+M
.
②充电完成时,Ni(OH)
2全部转化为NiO(OH).若继续充电将在一个电极产生O
2,O
2扩散到另一个电极发生电极反应被消耗,从而避免产生的气体引起电池爆炸,此时,阴极的电极反应式为
4MH+O2+4e-=2H2O+4M
4MH+O2+4e-=2H2O+4M
.




 (2011?四川模拟)A-M分别代表一种物质.其中,A、D、I、M的焰色反应呈紫色(透过蓝色钴玻璃),实验室常用I在MnO2催化作用下加热制备氧气;B、C是短周期元素组成的气体单质,且C为黄绿色;E是短周期元素组成的常见金属单质,它既能与D溶液反应,也能与G溶液反应.
(2011?四川模拟)A-M分别代表一种物质.其中,A、D、I、M的焰色反应呈紫色(透过蓝色钴玻璃),实验室常用I在MnO2催化作用下加热制备氧气;B、C是短周期元素组成的气体单质,且C为黄绿色;E是短周期元素组成的常见金属单质,它既能与D溶液反应,也能与G溶液反应.