
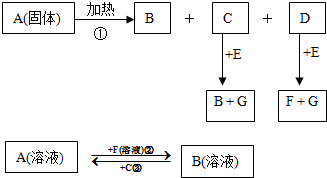
 ��ͼ��ʾ����ԲȦ�ཻ����Ӱ���ֱ�ʾԲȦ�ڵ�����������ķ�Ӧ����֪�Ƽ�������������ʵ�����Ϊ0.1mol��ˮ������Ϊ100g������˵����ȷ���ǣ�������
��ͼ��ʾ����ԲȦ�ཻ����Ӱ���ֱ�ʾԲȦ�ڵ�����������ķ�Ӧ����֪�Ƽ�������������ʵ�����Ϊ0.1mol��ˮ������Ϊ100g������˵����ȷ���ǣ�������| A��Na2O2����������������Ŀ֮��Ϊ1��1 |
| B����Ӧ������ܲ���0.05 mol O2 |
| C����Ӧ�ٵ����ӷ���ʽΪNa+2H2O�TNa++2OH-+H2�� |
| D���١��ڡ��۳�ַ�Ӧ��������Һ�����������Ӵ�С��˳��Ϊ�٣��ڣ��� |
| 1 |
| 2 |
| 1 |
| 2 |
| 4g |
| 100g+2.2g |
| 8g |
| 100g+6.2g |
| 8g |
| 100g+6.2g |


 ��ʿһ��ȫͨϵ�д�
��ʿһ��ȫͨϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������̫���ܡ�ˮ�ܡ����ܡ���ȼ��������Դ������ʹ��ú��ʯ�͵Ȼ�ʯȼ�� |
| B����ú�����������������ú���ۺ�����Ч�� |
| C����������ú��ʯ�ͣ���߲��������㹤ҵ�����Ŀ��ٷ�չ |
| D��ʵ����Դ�ġ�3R�����ùۣ�����������Դ���ģ�Reduce����������Դ���ظ�ʹ�ã�Reuse������Դ��ѭ��������Recycle�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ú�����������ҩ������θ����� |
| B�����մ��кͷ��������е��� |
| C���ô�����ϴ��ˮƿ�ڱڸ��ŵ�ˮ�� |
| D���ö�������Ѭ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���٢� | B���ڢ� | C���ڢ� | D���ܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ͭ | B���� | C��ʯӢ | D������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����̼��������Һ�У�K+��Al3+��SO42-��Cl- |
| B�����ڽ϶�Fe3+����Һ�У�Na+��SCN-��CO32-��K+ |
| C����������ˮ�������C��H+��ˮ?C��OH-��ˮ=10-24��Һ�У�NH4+��Cl-��CO32-��F- |
| D������ʹ��ɫʯ����ֽ����ɫ����Һ�У�Na+��S2-��NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��2L0.5mol?L-1�������Һ�����������������ΪNA |
| B��1molNa2O2 �����к���������Ϊ4NA |
| C���DZ�״���£�1molij�����������ԼΪ22.4L |
| D����״���£�22.4LNO��11.2LO2 �������ķ�������ԼΪ1.5NA �� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com