
【题目】有下列离子晶体空间结构示意图:●为阳离子,○为阴离子.以M代表阳离子,N代表阴离子,化学式为MN2的晶体结构为
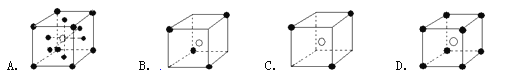
【答案】B
【解析】试题分析:A、阳离子位于顶点和面心,晶胞中总共含有阳离子数目为8×![]() +6×
+6×![]() =4,1个阴离子位于体心,为晶胞所独有,故晶胞中含有的阴离子数目为1,则阳离子和阴离子的比值为4:1,化学式为M4N,故A错误;B、有4个阳离子位于顶点,晶胞中平均含有阳离子数目为4×
=4,1个阴离子位于体心,为晶胞所独有,故晶胞中含有的阴离子数目为1,则阳离子和阴离子的比值为4:1,化学式为M4N,故A错误;B、有4个阳离子位于顶点,晶胞中平均含有阳离子数目为4×![]() =
=![]() ,1个阴离子位于体心,为晶胞所独有,故晶胞中含有的阴离子数目为1,则阳离子和阴离子的比值为
,1个阴离子位于体心,为晶胞所独有,故晶胞中含有的阴离子数目为1,则阳离子和阴离子的比值为![]() :1=1:2,化学式为MN2,故B正确;C、有3个阳离子位于顶点,晶胞中平均含有阳离子数目为3×
:1=1:2,化学式为MN2,故B正确;C、有3个阳离子位于顶点,晶胞中平均含有阳离子数目为3×![]() =
=![]() ,1个阴离子位于体心,为晶胞所独有,故晶胞中含有的阴离子数目为1,则阳离子和阴离子的比值为
,1个阴离子位于体心,为晶胞所独有,故晶胞中含有的阴离子数目为1,则阳离子和阴离子的比值为![]() :1=3:8,化学式为M3N8,故C错误;D、有8个阳离子位于顶点,晶胞中平均含有阳离子数目为8×
:1=3:8,化学式为M3N8,故C错误;D、有8个阳离子位于顶点,晶胞中平均含有阳离子数目为8×![]() =1,1个阴离子位于体心,为晶胞所独有,故晶胞中含有的阴离子数目为1,则阳离子和阴离子的比值为1:1,化学式为MN,故D错误;故选B。
=1,1个阴离子位于体心,为晶胞所独有,故晶胞中含有的阴离子数目为1,则阳离子和阴离子的比值为1:1,化学式为MN,故D错误;故选B。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】25℃时,向20mL0.1mol/LH2R溶液中滴加0.1mol/LNaOH溶液,溶液的pH随NaOH溶液体积的变化如图所示。已知pKa=-lgKa,二元弱酸H2R的pKa1=1.89,pKa2=7.21。下列有关说法不正确的是
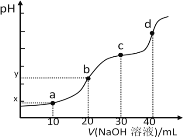
A.溶液的导电性:点a弱于点b
B.离子浓度c(R2-):点c大于点d
C.H2R+R2-=2HR-平衡常数>105,反应趋于完全
D.点b时,y<7且![]() <1
<1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.选取下列实验方法分离物质,将最佳分离方法的序号填在横线上。
A 萃取分液法 B 升华法 C 分液法 D 蒸馏法 E 过滤法
(1)_________分离饱和食盐水与沙子的混合物。
(2)_________分离水和汽油的混合物。
(3)_________分离四氯化碳(沸点为76.75 ℃)和甲苯(沸点为110.6 ℃)的混合物。
(4)_________分离碘水中的碘。
(5)_________分离氯化钠固体和碘固体的混合物。
II.图是甲、乙两种固体物质的溶解度曲线。
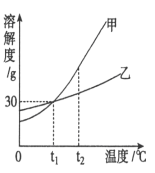
(1)t2℃时,将等质量的甲、乙两种物质加水溶解配制成饱和溶液,所得溶液质量的大小关系为:甲____________乙(填“>”、“<” 或 “=”)。
(2)除去甲物质中少量乙物质可采取____________结晶的方法(填“蒸发”或“降温”)。
III.如图装置,按要求填空
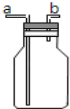
(1)排空气法收集气体,若收集CO2气体,进气口为__________(填“a”或“b”)
(2)若瓶中装满水,可用于收集下列气体中的__________(选填编号)
①NO ②NO2 ③NH3 ④HCl
(3)如果广口瓶中盛放浓硫酸,可以用作气体干燥装置,则该装置不可以干燥的气体有___________(选填编号)
①HCl ②H2 ③NH3 ④CO ⑤HI
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,Ksp(BaSO4)=1.0×10-10,Ksp(SrSO4)=3.0×10-7向20mL0.1mo1·L-1BaCl2溶液中滴加0.1mol·L-1的Na2SO4溶液,金属离子浓度与硫酸钠溶液体积的关系如图所示,已知:pM=-lgc(M2+)。下列说法正确的是( )
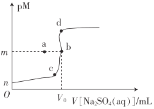
A.图像中,V0=20,m=5
B.在b点加少量BaCl2固体,Ksp(BaSO4)增大
C.若BaCl2溶液体积仍为20mL,浓度变为0.2mo1·L-1,则b点向a点迁移
D.若用SrCl2溶液替代BaCl2溶液,则b点向d点迁移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组利用下列化学反应在实验室中制备氯气,并进行有关氯气性质的研究。
![]()
(1)该小组同学欲用图所示仪器及试剂(不一定全用)制备并收集纯净、干燥的氯气。
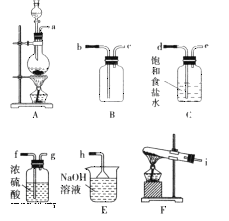
① 应该选择的仪器是__________(填字母)。
② 将各仪器按先后顺序连接起来,应该是a接__________,__________接__________,__________接__________,__________接h(用导管口处的字母表示)。
③ 浓盐酸与二氧化锰反应的离子方程式为__________。
(2)该小组同学设计分别利用图所示装置探究氯气的氧化性。
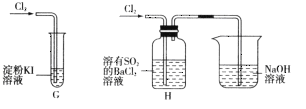
①G中的现象是__________,原因是__________(用化学方程式表示)。
②H中的现象是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
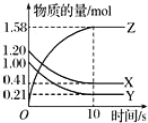
(1)写出该反应的化学方程式:___。
(2)列叙述中不能说明上述反应达到平衡状态的是___。
A.当X与Y的反应速率之比为1:1
B.在混合气体中X的质量百分数保持不变
C.混合气体的平均摩尔质量不随时间的变化而变化
D.混合气体的密度不随时间的变化而变化
E.X、Y、Z的浓度之比为1:1:2
(3)为使该反应的反应速率减小,可采取的措施是___。
A.恒压时充入Ne
B.适当升高温度
C.缩小容器的体积
D.选择高效催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是
A. Mg(OH)2(s)![]() MgCl2(aq)
MgCl2(aq)![]() Mg(s)
Mg(s)
B. FeCl2(aq)![]() FeCl3(aq)
FeCl3(aq)![]() Fe(OH)3(胶体)
Fe(OH)3(胶体)
C. 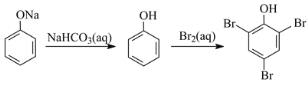
D. AgNO3(aq)![]() [Ag(NH3)2]+(aq)
[Ag(NH3)2]+(aq)![]() Ag(s)
Ag(s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向A、B、C和D四支试管中的溶液分别进行表中的操作,通过观察到的实验现象得出的结论正确的是( )
操作 | 现象 | 结论 | |
A | ①滴加稀HNO3 ②滴加BaCl2溶液 | 无明显现象白色沉淀 | 原溶液一定含SO |
B | 滴加稀盐酸 | 有大量气泡产生 | 原溶液一定含CO |
C | ①滴加稀HCl ②滴加AgNO3溶液 | 无明显现象白色沉淀 | 原溶液一定含Cl- |
D | ①加KSCN溶液 ②滴加氯水 | 无明显现象溶液呈红色 | 原溶液一定含Fe2+ |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com