
科目:高中化学 来源:2015-2016学年甘肃兰州一中高二上期中测试理科化学试卷(解析版) 题型:选择题
将固体A置于密闭容器中,在一定温度下发生下列反应:
①A(s)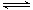 B(g)+C(g);②2C(g)
B(g)+C(g);②2C(g)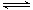 D(g)+E(g)。
D(g)+E(g)。
达到平衡时,c(D)=0.5mol·L-1,c(C)=4mol·L-1,则此温度下反应①的平衡常数为
A.25 B.20 C.16 D.9
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南洛阳高级中学高二上9月月考化学试卷(解析版) 题型:选择题
21世纪人类正由“化石能源时代”逐步向“多能源时代”过渡,下列不属于新能源的是
A.太阳能 B.核能 C.氢能 D.电力
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古巴彦淖尔高二上10月月考化学试卷(解析版) 题型:填空题
(10分)
如右图,一定温度下,分别往容积均为 5L 的甲(恒压容器)、乙(恒容容器)中加入 0.5mol无色的N2O4气体,立即出现红棕色。当反应进行到 2s时,测得乙容器中N2O4的浓度为 0.09mol·L-1。经过 60s,乙容器中的反应达到平衡。(反应过程中两个容器的温度均保持恒定)

(1)容器中气体出现红棕色的原因(用化学方程式表示)是: 。
(2)前 2s内乙容器中以N2O4的浓度变化表示的反应速率为 。
(3)达到平衡时,甲容器中反应所需的时间 60s(填“大于”、“小于”或“等于”,下同);容器内N2O4的浓度甲 乙;反应过程中吸收的能量甲 乙。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古巴彦淖尔高二上10月月考化学试卷(解析版) 题型:选择题
已知下列两个热化学方程式
2H2(g)+ O2(g)===2H2O(l)△H = -571.6kJ·mol-1
C3H8(g)+5O2(g)=== 3CO2(g)+ 4H2O(l)△H = -2 220.0kJ·mol-1
实验测得氢气和丙烷的混和气体共5 mol完全燃烧时放热3847kJ,则混和气体中氢气与丙烷的体积比是
A.1:3 B.3:1 C.1:4 D.1:1
查看答案和解析>>
科目:高中化学 来源:2016届湖北省高三上学期10月调考理综化学试卷(解析版) 题型:选择题
硝酸生产中,500℃时,NH3和O2可能发生如下反应:
① 4NH3 (g)+ 5O2 (g) 4NO (g)+ 6H2O (g)△H = -9072kJ·mol-1 K=1.1×1026
4NO (g)+ 6H2O (g)△H = -9072kJ·mol-1 K=1.1×1026
② 4NH3 (g)+ 4O2 (g) 2N2O (g)+ 6H2O (g)△H=-1104.9kJ·mol-1 K=4.4×1028
2N2O (g)+ 6H2O (g)△H=-1104.9kJ·mol-1 K=4.4×1028
③ 4NH3 (g)+ 3O2 (g) 2N2 (g)+ 6H2O (g)△H=-1269.02kJ·mol-1 K=7.1×1034
2N2 (g)+ 6H2O (g)△H=-1269.02kJ·mol-1 K=7.1×1034
其中,②、③是副反应。若要减少副反应,提高单位时间内NO的产率,最合理的措施是
A.增大O2浓度 B.使用合适的催化剂 C.减小压强 D.降低温度
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上学期第一次月考化学试卷(解析版) 题型:选择题
下表中是各组反应的反应物和温度,反应刚开始时,放出H2速率最快的是
金属(粉末状)(mol) | 酸的浓度及体积 | 反应温度(℃) | |
A | Mg 0.1 | 0.1 6 mol·L-1硝酸10mL | 80 |
B. | Mg 0.1 | 0.1 3 mol·L-1盐酸10mL | 60 |
C. | Fe 0.1 | 0.1 3 mol·L-1盐酸10mL | 60 |
D. | Mg 0.1 | 0.1 3 mol·L-1硫酸10mL | 60 |
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省高三上学期第二次检测化学试卷(解析版) 题型:选择题
已知25 ℃下,Ka(HCOOH)=1.78×10-4,Kb(NH3·H2O)=1.79×10-5。保持25 ℃不变,向一定体积0.1 mol·L-1 的氨水中滴加0.1 mol·L-1 的甲酸溶液。在滴加过程中
A.水的电离常数先增大后减小
B.当氨水和甲酸溶液体积相等时,c(HCOO-)=c(NH4+)
C.c(NH3·H2O)与c(NH4+)之和始终保持不变
D. 始终保持不变
始终保持不变
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一上第二次月考化学试卷(解析版) 题型:选择题
溶液、胶体和浊液这三种分散系的本质区别是北京四中网校
A.是否有丁达尔现象 B.是否能透过滤纸
C.分散质粒子直径的大小 D.是否均一、透明、稳定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com