
| A、CuSO4溶液吸收H2S气体:Cu2++H2S→CuS↓+2H+ | ||
B、Ca(HCO3)2溶液和少量的NaOH溶液混合:Ca2++2HC
| ||
| C、硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液:Fe2++2H++H2O2→Fe2++2H2O | ||
| D、淀粉碘化钾溶液在空气中变蓝:4I-+O2+2H2O→2I2+4OH- |


科目:高中化学 来源: 题型:
| A、H+、SO42-、SO32- |
| B、Ba2+、CO32-、NO3- |
| C、Na+、Cl-、SO42- |
| D、Ca2+、SO42-、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
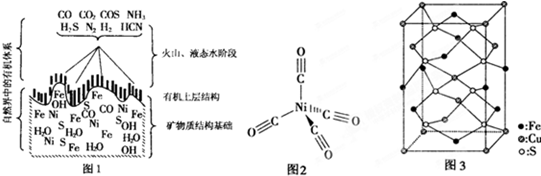
| 2 |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 化学在能源开发与利用中起到十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.
化学在能源开发与利用中起到十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.
| ||
| 时间(h) 物质的量(mol) |
0 | 1 | 2 | 3 | 4 |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0.00 | 0.20 | n2 | 1.00 | 1.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、FeBr2与Cl2 |
| B、C6H5ONa与CO2 |
| C、HCl与Na2CO3 |
| D、Ca(HCO3)2与NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用石英与烧碱溶液反应制备防火剂硅酸钠溶液:SiO2+2OH-=SiO32-+H2O |
| B、用食醋检验牙膏中的摩擦剂碳酸钙:CaCO3+2H+=Ca2++H2O+CO2↑ |
| C、用氯化铁溶液腐蚀铜线路板:Cu+Fe3+=Cu2++Fe2+ |
| D、用氢氧化钠溶液去除铝表面的氧化膜:Al2O3+2OH-=2AlO2-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com