
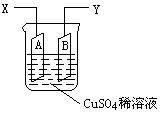
 6min后,假设溶液体积不变,测得溶液中CuSO4物质的量浓度为0.1mol/L,则原溶液中CuSO4物质的量浓度 mol/L。溶液中H+的物质
6min后,假设溶液体积不变,测得溶液中CuSO4物质的量浓度为0.1mol/L,则原溶液中CuSO4物质的量浓度 mol/L。溶液中H+的物质 mol/L。
mol/L。 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:实验题
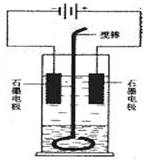
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.3.36L | B.2.8L | C.6.72L | D.4.48L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电解精炼铜时,同一时间内阳极溶解的粗铜的质量比阴极析出的铜的质量大 |
| B.在镀件上电镀锌,可以用锌做阳极,也可以用惰性材料做阳极 |
| C.二次电池充电过程是化学能转化为电能的过程 |
| D.二次电池充电时,电池上标有“+”的电极应与外接电源的负极相连 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
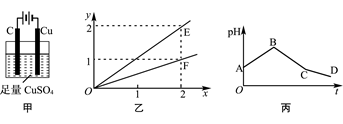
| A.E表示反应生成Cu的物质的量 |
| B.F表示反应生成H2SO4的物质的量 |
| C.BC段阳极产物是Cl2 |
| D.CD段电解的物质是水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
 息(Ⅰ、Ⅱ两极分别代表两极各自产生的气体体积),通过计算推测:
息(Ⅰ、Ⅱ两极分别代表两极各自产生的气体体积),通过计算推测: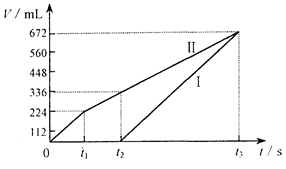
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.Cl2 | B.O2 | C.H2 | D.HCl |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
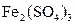 和
和 的混合液,且已知
的混合液,且已知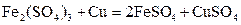 ,下列说法正确的是
,下列说法正确的是A.阴极反应式为: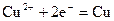 ,当有 ,当有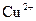 存在时 存在时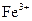 不放电 不放电 |
| B.阴极上首先析出铁,然后析出铜 |
| C.阴极上不可能析出铜 |
D.首先被电解的是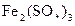 和 和 ,后被电解的是 ,后被电解的是 和 和 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com