
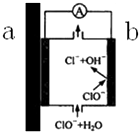
 自来水管道经历了从铸铁管→镀锌管→PVC管→PPR热熔管等阶段,铸铁管、镀锌管被弃用的原因之一,可以用原电池原理来解释,示意图如图所示,下列有关说法不正确的是( )
自来水管道经历了从铸铁管→镀锌管→PVC管→PPR热熔管等阶段,铸铁管、镀锌管被弃用的原因之一,可以用原电池原理来解释,示意图如图所示,下列有关说法不正确的是( )| A. | 如果是镀锌管,则a端为Zn,是负极,产生Zn2+,不但会造成管道锈蚀,Zn2+溶于自来水也对人体有害 | |
| B. | b端发生的电极反应为:ClO-+H2O-2e-═Cl-+2OH- | |
| C. | 由于该原电池原理的存在,一定程度上减弱了自来水中余氯的杀菌消毒功能 | |
| D. | 从自来水厂到用户,经过该类管道的长期接触,自来水的酸碱性发生了变化 |
分析 根据装置图,b端次氯酸根得电子发生还原反应生成氯离子,所以b端为正极电极反应为:ClO-+H2O+2e-═Cl-+2OH-,则a端为负极,据此分析.
解答 解:根据装置图,b端次氯酸根得电子发生还原反应生成氯离子,所以b端为正极,则a端为负极,
A、如果是镀锌管,锌比铁活泼,则a端负极为Zn,产生Zn2+,Zn2+溶于自来水也对人体有害,故A正确;
B.b端为正极,电极反应为:ClO-+H2O+2e-═Cl-+2OH-,故B错误;
C.根据正极电极反应为:ClO-+H2O+2e-═Cl-+2OH-,则消耗了次氯酸根,所以一定程度上减弱了自来水中余氯的杀菌消毒功能,故C正确;
D.根据正极电极反应为:ClO-+H2O+2e-═Cl-+2OH-,所以经过该类管道的长期接触,自来水的酸碱性发生了变化,故D正确;
故选B.
点评 本题考查了原电池原理,根据得失电子的难易程度确定正负极,再结合电子移动方向来分析解答,题目难度不大.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3-氯戊烷的分子式为C5H9Cl3 | B. | 3-氯戊烷属于烷烃 | ||
| C. | 3-氯戊烷能发生取代反应 | D. | 3-氯戊烷的同分异构体共有6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 食醋中含有的醋酸 | B. | 酒中含有的酒精 | ||
| C. | 葡萄中含有的葡萄糖 | D. | 谷类中含有的淀粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 放电时负极反应为:3Zn-6e-═3Zn2+ | |
| B. | 放电时正极反应为:2FeO42-+6e-+8H2O═2Fe(OH)3+10OH- | |
| C. | 放电时每转移3mol电子,正极有1mol K2FeO4被氧化 | |
| D. | 放电时负极附近溶液的碱性减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
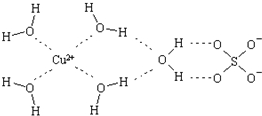 科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如下,其中配位键和氢键均采用虚线表示.
科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如下,其中配位键和氢键均采用虚线表示.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
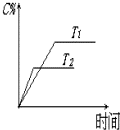 可逆反应aA(s)+bB(g)?c C(g)+d D(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)如图.下列叙述一定正确的是B
可逆反应aA(s)+bB(g)?c C(g)+d D(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)如图.下列叙述一定正确的是B查看答案和解析>>
科目:高中化学 来源: 题型:解答题
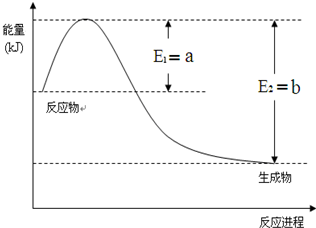 运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义
运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | HCOOH | CH3OH | HCOOCH3 |
| 主要 性质 | 无色液体,与水互溶 K(HCOOH)>K(CH3COOH) | 无色液体,与水互溶 | 无色液体,在水中溶解度小,与醇互溶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com