
在钢铁腐蚀过程中,下列五种变化可能发生的是
①Fe2+转化为Fe3+ ②O2被还原 ③产生H2 ④Fe(OH)3失水形成Fe2O3·H2O ⑤杂质碳被氧化
A.只有①和② B.只有②③④ C.①②③④ D.①②③④⑤
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:高中化学 来源: 题型:
目前,新能源不断被应用到现代的汽车中,高铁电池技术就是科研机构着力研究的一个方向。
(1)高铁酸钾锌电池(碱性介质)是一种典型的高铁电池,则该种电池负极材料是________。
(2)工业上常采用NaClO氧化法生产高铁酸钾(K2FeO4),K2FeO4在碱性环境中稳定,在中性和酸性条件下不稳定。反应原理为
Ⅰ.在碱性条件下,利用NaClO氧化Fe(NO3)3制得Na2FeO4
3NaClO+2Fe(NO3)3+10NaOH===2Na2FeO4↓+3NaCl+6NaNO3+5H2O
Ⅱ.Na2FeO4与KOH反应生成K2FeO4
Na2FeO4+2KOH===K2FeO4↓+2NaOH
主要的生产流程如下:

①写出反应①的离子方程式________________________________________________。
②流程图中“转化”(反应③)是在某低温下进行的,且此温度无NaOH析出,说明此温度下Ksp(K2FeO4)____Ksp(Na2FeO4)(填“>”、“<”或“=”)。
(3)已知K2FeO4在水溶液中可以发生:__FeO +__H2O__Fe(OH)3↓+__OH-+__O2↑,配平上述方程式K2FeO4在水处理中的作用是__________________。
+__H2O__Fe(OH)3↓+__OH-+__O2↑,配平上述方程式K2FeO4在水处理中的作用是__________________。
(4)FeO 在水溶液中的存在形态如图所示:
在水溶液中的存在形态如图所示:

①若向pH=10的这种溶液中加硫酸至pH=2,HFeO 的分布分数的变化情况是________。
的分布分数的变化情况是________。
②若向pH=6的这种溶液中滴加KOH溶液,则溶液中含铁元素的微粒中,________转化为____________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
小明为验证NO2的氧化性和NO的还原性,设计了如下装置制取NO2和NO,并验证其性质,装置图如下:
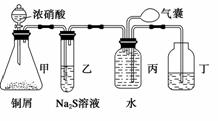
(1)写出甲中反应的离子方程式:______________________________________________
________________,乙中的现象是__________________________________________,
可证明NO2的氧化性;在丙中鼓入空气后现象是_______________________________
________________________________________________________________________,可证明NO的还原性。
(2)实验前丙中充满水的作用是_______________________________________________
________________________________________________________________________
(用反应方程式和简要文字回答)。
(3)小华对小明的实验设计提出了质疑,他认为乙中的现象不足以证明NO2的氧化性,他的理由是_________________________________________________________________
________________________________________________________________________。
你认为怎样才能准确证明NO2的氧化性?(简要回答出原理和现象即可)____________
____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
为了测定中和反应的反应热,计算时至少需要的数据是
①酸的浓度和体积 ②碱的浓度和体积 ③比热容 ④反应后溶液的质量 ⑤生成水的物质的量 ⑥反应前后溶液温度变化 ⑦操作所需的时间
A.①②③⑥ B.①③④⑥
C.③④⑤⑥ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,发生CO + NO2  CO2 + NO 的反应,达到化学平衡后,降低温度,混合物的颜色变浅,下列有关该反应的说法中正确的是
CO2 + NO 的反应,达到化学平衡后,降低温度,混合物的颜色变浅,下列有关该反应的说法中正确的是
A.正反应为吸热反应 B.正反应为放热反应
C.降温后CO的浓度增大 D.降温后各物质的浓度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
化学是一门实用性强的自然科学,在社会、生产、生活中起着重要的作用,下列说法正确的是
A.金属钠具有强还原性,可用与TiCl4溶液反应制取金属Ti
B. 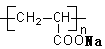 表示一种吸水性高分子树脂
表示一种吸水性高分子树脂
C.用于现代建筑的钢筋混凝土不属于复合材料
D.山东东营广饶县一男子收到网购物品后,因吸入氟乙酸甲酯中毒身亡,氟乙酸甲酯的结构
简式为FCH2COOCH3,能与H2发生加成反应,也能被LiAlH4还原
查看答案和解析>>
科目:高中化学 来源: 题型:
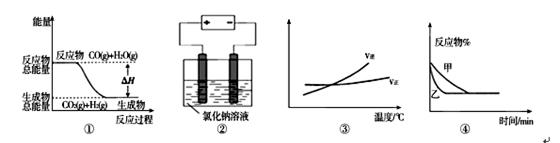
关于下列四个图象的说法中正确的是 ( )
A.图①表示可逆反应“CO(g)+H2O(g) CO2(g)+H2(g)”中的△H大于0
CO2(g)+H2(g)”中的△H大于0
B.图②是在电解氯化钠稀溶液的电解池中,阴、阳极产生气体体积之比一定为1:1
C.图③表示可逆反应“A2(g)+3B2(g) 2AB3(g)”的△H小于0
2AB3(g)”的△H小于0
D.图④表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强大
3C(g)+D(s)的影响,乙的压强大
查看答案和解析>>
科目:高中化学 来源: 题型:
有Fe2+、NO3-、Fe3+、NH4+、H+、H2O六种微粒,分别属于一个氧化还原反应中的反应物和生成物,下列叙述不正确的是( )
A.氧化剂中心原子的杂化方式为sp2
B.还原剂的外围电子排布式为3d54s1
C.还原产物的VSEPR模型为正四面体
D.该反应可设计为原电池,其负极反应为Fe2+- e-= Fe3+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com