
| ���� |
| ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c��NO��/mol?L-1 | 1.00��10-3 | 4.50��10-4 | 2.50��10-4 | 1.50��10-4 | 1.00��10-4 | 1.00��10-4 |
| c��CO��/mol?L-1 | 3.60��10-3 | 3.05��10-3 | 2.85��10-3 | 2.75��10-3 | 2.70��10-3 | 2.70��10-3 |
| 1.00��10-3-2.5��10-4 |
| 2s |
| ���� |
| c(N2)c2(CO2) |
| c2(CO)c2(NO) |
| (4.50��10-4)?(9��10-4)2 |
| (1.00��10-4)2?(2.7��10-3)2 |
| 256.6kJ |
| 0.4 |


 �̲�ȫ���ִʾ�ƪϵ�д�
�̲�ȫ���ִʾ�ƪϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015��㶫ʡ�����и߶���ѧ����ĩ��ѧ������⻯ѧ�Ծ��������棩 ���ͣ������
���������ǿ�������Ҫ��Ⱦ���������������Ⱦ�ж��ַ������ô������ɽ������ٷɻ�β���е�NO��COת���CO2��N2���䷴ӦΪ��2NO��2CO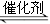 2CO2��N2��Ϊ�˲ⶨ��ij�ִ��������µķ�Ӧ���ʣ���ij�¶��²�ò�ͬʱ���NO��COŨ�����±���
2CO2��N2��Ϊ�˲ⶨ��ij�ִ��������µķ�Ӧ���ʣ���ij�¶��²�ò�ͬʱ���NO��COŨ�����±���
|
ʱ�䣨s�� |
0 |
2 |
4 |
|
c��NO�� �� mol��L��1�� |
1.00��10��3 |
2.50��10��4 |
1.00��10��4 |
|
c��CO�� �� mol��L��1�� |
3.60��10��3 |
c�� |
2.70��10��3 |
�ش��������⣨���������¶ȱ仯�Դ�����Ч�ʵ�Ӱ�죩��
��1��ǰ4s�ڵ�ƽ����Ӧ����v��NO���� ��c���� ��
��2��������һ��ʱ�������������ı���������ѧ��Ӧ���ʡ���ͼ��ʾ��������������ʱ��������Ӧ�ж�����̼Ũ�����¶ȣ�T���������������S����ʱ�䣨t���ı仯���ߡ�

�ٸ÷�Ӧ�Ħ�H 0�����������������������
���������ı����S1��S2���ڴ��ͼ�л���c��CO2�� ��T2��S2�����´ﵽƽ������еı仯���ߡ�
��3���ں��ݵ��ܱ������У�������Ӧ�ﵽƽ��ı�ijһ����������ʾ��ͼ��ȷ����

A�� B�� C�� D��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ������ʡ��˳����У�����������ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
�����仯����������������������е���ϵ��������һ֧15mL���Թܣ�����NO������ˮ���У����Թ��л���ͨ��һ�������������Թ���Һ���ȶ�ʱ��ʣ������3mL����ͨ���������������Ϊ mL��
��Ŀǰ����������������Ⱦ�ж��ַ�����
��1����CH4����ԭ��������������������������Ⱦ����֪��
��CH4(g)+4NO2(g)= 4NO(g)+CO2(g)+2H2O(g) ��H=-574kJ/mol
��CH4(g)+4NO(g)= 2N2(g)+CO2(g)+2H2O(g) ��H=-1160kJ/mol
��H2O(g)= H2O(l) ��H=-44kJ/mol
д��CH4(g)��NO2(g)��Ӧ����N2(g) ��CO2(g)��H2O(l)���Ȼ�ѧ����ʽ ��
��2���û���̿��ԭ��������������йط�ӦΪ��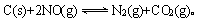
ij�о�С��������ܱ���������һ�����Ļ���̿��NO�����£�T0C)�����·�Ӧ����Ӧ���е���ͬʱ���ø����ʵ�Ũ�����£�
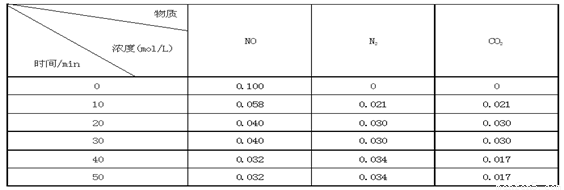
�ٲ�����Ϊ�жϷ�Ӧ�ﵽ��ѧƽ��״̬��������_______ ����ѡ����ĸ���ţ�
A��������CO2��Ũ�ȱ��ֲ���
B��v��(N2)=2 v��(NO)
C��������ѹǿ���ֲ���
D�����������ܶȱ��ֲ���
E����������ƽ����Է����������ֲ���
��ǰ20���ӣ�ƽ����Ӧ����v(NO)= ��v(NO)=��0��1- 0��04��/ 20 = 0��003mol��L-1�� min-1
����T0Cʱ���÷�Ӧ��ƽ�ⳣ��Ϊ_______(������λС��)��
����30 min���ı�ijһ������Ӧ���´ﵽƽ�⣬��ı��������_______ ��
��3����ѧ�������о����ô������������ٷɻ�β���е�NO��COת���CO2��N2,�䷴ӦΪ��
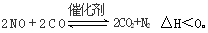
�о���������ʹ�õ���������ʱ����������ıȱ���������ѧ��Ӧ���ʡ�Ϊ�˷ֱ���֤�¶ȡ������ıȱ�����Ի�ѧ��Ӧ���ʵ�Ӱ����ɣ�ijͬѧ���������ʵ�飬����ʵ�������Ѿ������±��С�
|
ʵ���� |
T(0C) |
NO��ʼŨ�� ��mol/L�� |
CO��ʼŨ�� ��mol/L�� |
�����ı� �����(m2/g) |
|
�� |
280 |
1��20��10-3 |
5��80��10-3 |
82 |
|
�� |
a |
b |
c |
124 |
|
�� |
350 |
d |
e |
124 |
�ϱ��У�a=_______,b=________,e=________ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ�����ʡ�人�и������µ��в��������ۺϻ�ѧ�Ծ��������棩 ���ͣ������
Ŀǰ����������������Ⱦ�ж��ַ�����
��1����CH4����ԭ��������������������������Ⱦ����֪��
��CH4(g)��4NO2(g)��4NO(g)��CO2(g)��2H2O(g) ��H����574 kJ��mol��1
��CH4(g)��4NO(g)��2N2(g)��CO2(g)��2H2O(g) ��H����1160 kJ��mol��1
��H2O(g)��H2O(l) ��H����44��0 kJ��mol��1
д��CH4 (g)��NO2 (g)��Ӧ����N2 (g) ,CO2(g)��H2O(l)���Ȼ�ѧ���� ʽ_____________________
��2���û���̿��ԭ��������������йط�ӦΪ��C(s)��2NO(g)  N2(g)��CO2(g)ij�о�С��������ܱ���������һ�����Ļ���̿��NO�����£�T��C)�����·�Ӧ����Ӧ���е���ͬʱ���ø����ʵ�Ũ������
N2(g)��CO2(g)ij�о�С��������ܱ���������һ�����Ļ���̿��NO�����£�T��C)�����·�Ӧ����Ӧ���е���ͬʱ���ø����ʵ�Ũ������
�ٲ�����Ϊ�жϷ�Ӧ�ﵽ��ѧƽ��״̬������ ��_______
A��������CO2��Ũ�ȱ��ֲ���
B��v����N2��=2 v����NO��
C��������ѹǿ���ֲ���
D�����������ܶȱ��ֲ���
E����������ƽ����Է����������ֲ���
����T��Cʱ���÷�Ӧ��ƽ�ⳣ��Ϊ_______(������λС��)��
����30 min,�ı�ijһ����,��Ӧ���´ﵽƽ��,��ı��������_______
��3����ѧ�������о����ô������������ٷɻ�β���е�NO��COת���CO2��N2,�䷴ӦΪ��
2CO��2NO  N2��2CO2 ��H<0 �о���������ʹ�õ���������ʱ����������ıȱ���������ѧ��Ӧ���ʣ�Ϊ�˷ֱ���֤�¶ȡ������ıȱ�����Ի�ѧ�� Ӧ���ʵ�Ӱ����ɡ�ijͬѧ���������ʵ�飬����ʵ�������Ѿ������±��С�
N2��2CO2 ��H<0 �о���������ʹ�õ���������ʱ����������ıȱ���������ѧ��Ӧ���ʣ�Ϊ�˷ֱ���֤�¶ȡ������ıȱ�����Ի�ѧ�� Ӧ���ʵ�Ӱ����ɡ�ijͬѧ���������ʵ�飬����ʵ�������Ѿ������±��С�

���ϱ���:a=_______,b=________,e=________
�����ڸ���������ͼ�У������ϱ���ʵ��II��ʵ��III�����»��������NOŨ����ʱ��仯����������ͼ,��������Ӧ��ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
I���ɻ�β���е�NO���ƻ������㡣���ô�
������ʹβ���е�NO��CO������Ӧ2NO +2CO![]() 2CO2��+N2����H<0����֪��������ȱ���������ѧ��Ӧ���ʡ�Ϊ�˷ֱ���֤�¶ȡ������ȱ�������Ի�ѧ��Ӧ���ʵ�Ӱ����ɣ�ijͬѧ���������ʵ�飬����ʵ�������Ѿ���������ʵ����Ʊ���
2CO2��+N2����H<0����֪��������ȱ���������ѧ��Ӧ���ʡ�Ϊ�˷ֱ���֤�¶ȡ������ȱ�������Ի�ѧ��Ӧ���ʵ�Ӱ����ɣ�ijͬѧ���������ʵ�飬����ʵ�������Ѿ���������ʵ����Ʊ���
ʵ���� | T���棩 | NO��ʼŨ�ȣ�mol/L�� | CO��ʼŨ�ȣ�mol/L�� | �����ıȱ������m2/g�� |
�� | 280 | 1.20��10-3 | 5.80��10-3 | 82 |
�� | 1.20��10-3 | 124 | ||
�� | 350 | 5.80��10-3 |
�� ��1������ȫ���еĸ��ո�
�� ��2�������ұ߸���������ͼ�У������ϱ��е���
 ��ʵ�������»��������NOŨ����ʱ���
��ʵ�������»��������NOŨ����ʱ���
������������ͼ���������������ߵ�ʵ���š�
II��������ȼ������ʱ�����ĸ��»�����N2��O2�ķ�Ӧ��
N2��g��+O2��g��![]() =2NO��g���ǵ�������β���к���NO��ԭ��֮һ��
=2NO��g���ǵ�������β���к���NO��ԭ��֮һ��
2000Cʱ�����ݻ�Ϊ2L���ܱ������г���10molN2��5mol O2���ﵽƽ���NO�����ʵ���Ϊ2mol����÷�Ӧ��ƽ�ⳣ��K=___ ���������� _ �����¶��£�����ʼʱ�����������г���1 molN2��һ������O2��ƽ��ʱO2��NO�����ʵ���ǡ����ȣ���ƽ ��ʱN2�����ʵ����������� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com