
【题目】(2017·安徽省蒙城一中高一下学期第一次月考)为除去KCl溶液中含有的少量K2SO4和CaCl2,下列各操作:①加热蒸发;②加过量BaCl2溶液;③加适量盐酸;④加过量K2CO3;⑤过滤。顺序正确的是
A.②③④⑤① B.②④⑤③① C.①②③④⑤ D.④③②⑤①
科目:高中化学 来源: 题型:
【题目】如图装置中,U型管内为红墨水,a、b试管中分别盛有食盐水和氯化铵溶液(已知氯化铵溶液呈酸性),各加入生铁块,放置一段时间.下列有关描述错误的是( ) 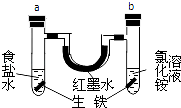
A.a中发生了吸氧腐蚀,b中发生了析氢腐蚀
B.a中正极反应方程式是:O2+2H2O+4e﹣═4OH﹣
C.a、b试管中生铁块中铁都作电池的负极
D.红墨水在一段时间后,两边液面变为左低右高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列相关问题:
(1)用“>”或“<”填写下表:
电负性 | 第一电离能 | 半径 | 金属性 | 杂化轨道数 |
Al___Mg | S___P | Na+___O2- | Pb___Sn | SO2____SO32- |
(2)某半导体材料由X、Y两种元素组成,已知X的基态原子4p轨道上只有1个电子,Y的基态原子L层上有3个未成对电子,X位于周期表第_____周期____族;该半导体材料的化学式为_____。
(3)在短周期元素中基态原子的p轨道有1个未成对电子的元素可能是____(填元素符号),其中核电荷数最大的元素核外电子排布式是________。
(4)雷式盐(Reinecke’s salt)结构式如下图所示:

配离子中Cr3+的配体为____(填化学式),Cr3+与配体间形成的共价键又称为____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近中国科学院上海高等研究院在合成气直接制烯烃研究获重大突破.已知:
反应①:C(s)+ ![]() O2(g)=CO (g)△H1
O2(g)=CO (g)△H1
反应②:C(s)+H2O(g)=CO(g)+H2(g)△H2
反应③:CO(g)+2H2(g)=CH3OH(g)△H 3=﹣90.1kJmol﹣1
反应④:2CH3OH(g)=CH3OCH3(g)+H2O(g)△H 4=﹣134.0kJmol﹣1
反应⑤:3CH3OH(g)=CH3CH=CH2(g)+3H2O(g)△H 5=﹣31.0kJmol﹣1
下列说法正确的是( )
A.△H1﹣△H2<0
B.反应②为放热反应
C.3CH3OCH3(g)=2CH3CH=CH2(g)+3H2O(g)△H=﹣103.0 kJmol﹣1
D.3CO(g)+6H2(g)=CH3CH=CH2(g)+3H2O(g)△H=﹣301.3kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X,Y,Z,W在元素周期表中的相对位置如图所示,其中Z所处的族序数是周期序数的2倍.下列判断不正确的是( ) ![]()
A.最高正化合价:X<Y<Z
B.原子半径:X<Y<Z
C.气态氢化物的热稳定性:Z<W
D.最高价氧化物对应水化物的酸性:X<Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从含铜废料(如:覆铜板、印刷线路板及铅冰铜等)中提取铜,既可提高资源的利用率又可减少重金属污染.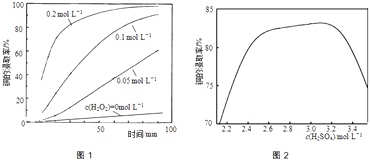
(1)废覆铜板(Cu和Sn组成)可用CuSO4和H2SO4混合溶液作电解质溶液,直接电解回收精铜,阳极上发生的电极反应为 .
(2)废印刷线路板中的铜常用含盐酸的FeCl3溶液或H2O2﹣HCl﹣NaCl混合溶液浸取回收.
①用FeCl3溶液浸取铜时发生反应的离子方程式为;若加盐酸不足,反应一段时间后线路板表面有红褐色沉淀,产生红褐色沉淀的原因是 .
②将粉碎后的废印刷线路板放入三口烧瓶中,分别加入由0.3molL﹣1盐酸、0.5molL﹣1NaCl及不同浓度的H2O2组成的混合溶液,在温度、搅拌速率及固液比等均相同时,铜的浸取率随H2O2的浓度和时间的变化如图1所示.当c(H2O2)=0molL﹣1时,也有少量的铜被浸出,其原因是 .
③用H2O2﹣HCl﹣NaCl混合溶液浸取时,其浸取过程包括:
(Ⅰ) Cu+H2O2+2H+=Cu2++2H2O
(Ⅱ) Cu2++Cu2Cu+
(Ⅲ) Cu++nCl﹣CuCln(n﹣1)﹣
(Ⅳ) 2CuCln(n﹣1)﹣+2H++H2O2=2Cu2++2H2O+2nCl﹣
其他条件相同时,增大下列离子浓度可以加速Cu从废电路板中浸出的是(填序号).
a.Na+ b.Cu2+ c.Cl﹣d.OH﹣
(3)铅冰铜(PbS、Cu2S及FeS的混合物)可用HCl﹣H2O2混合溶液浸取.
①Cu2S被HCl﹣H2O2混合溶液浸取得到硫酸铜和氯化铜溶液的化学方程式为 .
②若由H2SO4代替HCl﹣H2O2中的HCl,其他条件相同,铜的浸取率随硫酸浓度的变化如图2所示.当H2SO4浓度大于3.1molL﹣1时,硫酸浓度越大,铜的浸取率反而越小,其原因可能是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关氨或铵盐的说法不正确的是( )
A.NH3属于弱电解质
B.可用湿润的红色石蕊试纸检验氨气
C.用盐酸滴定氨水,当溶液呈中性时,c(NH4+)=c(Cl﹣)
D.常温时,0.1mol?L﹣1NH4Cl溶液加水稀释, ![]() 的值不变
的值不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com