
���� ��1�����ݶ�����̼����������֮��Ķ�����ϵ�����жϷ�Ӧ�����з����ķ�Ӧ�������������̼������������Һ��Ӧ����̼���ƺ�ˮ������������̼������������Һ��Ӧ����̼�����ƺ�ˮ��
��2���ڢ��������Һ��Ŀ���ǸϾ���Һ�ж�����̼��
��3���ڢ��л����һ��NaOH��Һ�����ķ�Ӧ��̼�����ƺ��������Ʒ�Ӧ����̼���ƣ�
��� �⣺��1���������ƺ���������̼��Ӧ����̼�����ƣ���Ӧ�����Ƕ�����̼������������Һ��Ӧ����̼������Һ����Ӧ�����ӷ���ʽΪ��CO2+2OH-=CO32-+H2O��������Ӧ��������̼��̼���Ʒ�Ӧ����̼��������Һ����Ӧ�����ӷ���ʽΪ��CO2+CO32-+H2O=2HCO32-��
�ʴ�Ϊ��CO2+2OH-=CO32-+H2O��CO2+CO32-+H2O=2HCO32-��
��2���ڢ��������Һ��Ŀ���Ǹ����ܽ�����Һ�е�CO2���壬��ֹ̼�����Ʒֽ⣬������������Һ���ܽ��CO2���壬����ۼ����NaOH���в�����CO2��Ӧ�����ĵ���ʹNaHCO3������ȫת����Na2CO3��
�ʴ�Ϊ�������ܽ�����Һ�е�CO2���壬��ֹ̼�����Ʒֽ⣻
��3���ڢ��л����һ��NaOH��Һ�����ķ�Ӧ�����ӷ���ʽ��̼�������ܺ��������Ʒ�Ӧ����̼���ƺ�ˮ����Ӧ���ӷ���ʽΪHCO3-+OH-�TCO32-+H2O��
�ʴ�Ϊ��HCO3-+OH-�TCO32-+H2O��
���� ���⿼�����Ƶ���Ҫ����������ʣ������Ʊ���ʵ�鷽������������ͬ���ﲻͬ��ע��֪ʶ���ۣ���Ŀ�Ѷ��еȣ�


 �·Ƿ��̸����100��ϵ�д�
�·Ƿ��̸����100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ����Ʒ�� | �������ͯ���� | ����������� | �л������� |
| Ħ���� | �������� | ̼��� | �������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������Ż�ʱʹ����ĭ�������� | |
| B�� | ���Թܼ���̼�����ƹ���ʱʹ�Թܿ���ֱ���� | |
| C�� | ����ʵ��ʱ������ƿ�з��뼸����ʯ�������Ƭ�� | |
| D�� | Ũ���ὦ��Ƥ����ʱ������ϡ����������Һ��ϴ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ʯ������裾�������裾̼���� | B�� | H2Te��H2Se��H2S��H2O | ||
| C�� | MgO��NaCl��H2O��HF | D�� | ���ʯ���������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��1��ijϩ�������������ӳɷ�Ӧ�ɵõ��ṹ��ʽ����ͼ�������������ϩ�����ܵĽṹ��ʽ�ǣ�CH2=CHCH3CHCH3C��CH3��3����CH3��2C=CCH3C��CH3��3����CH3��2CHC=CH2C��CH3��3��
��1��ijϩ�������������ӳɷ�Ӧ�ɵõ��ṹ��ʽ����ͼ�������������ϩ�����ܵĽṹ��ʽ�ǣ�CH2=CHCH3CHCH3C��CH3��3����CH3��2C=CCH3C��CH3��3����CH3��2CHC=CH2C��CH3��3��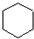 ��E��CH3CH3��
��E��CH3CH3��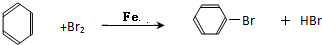 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | X�ķǽ�����ǿ��W | |
| B�� | X��Y���γɵ����ӻ����ﲻֹһ�� | |
| C�� | WԪ������������Ӧˮ����Ļ�ѧʽΪH2WO4 | |
| D�� | Y��Z�ļ����Ӷ����ƻ�ˮ�ĵ���ƽ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ����� | B�� | ˮ���� | C�� | ���� | D�� | Ư�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��ѧ�� | C-H | H-H | C-O | H-O |
| ����/kJ•mol-l | 413 | 436 | 343 | 465 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaOH | B�� | HCl | C�� | Ca��OH��2 | D�� | Na2O2 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com