
下列离子方程式中,属于水解反应的是( )
A.CH3COOH +H2O  CH3COO- + H3O+
CH3COO- + H3O+
B.SO2 + H2O  HSO3- + H+
HSO3- + H+
C.HS- + H2O  S2- + H3O+
S2- + H3O+
D.CO32- + H2O  HCO3- + OH-
HCO3- + OH-
科目:高中化学 来源: 题型:
0.02mol氯化铬(CrCl3·6H2O)在水溶液中用过量的AgNO3处理,产生0.04mol AgCl沉淀,此氯化铬最可能形成的是( )
A.[Cr(H2O)6]Cl3 B.[Cr(H2O)3Cl3]·3H2O
C.[Cr(H2O)4Cl2]Cl·2H2O D.[Cr(H2O)5Cl]Cl2·H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
碳、氮、硫是中学化学重要的非金属元素,在工农业生产中有广泛的应用。
 (1)用于发射“天宫一号”的长征二号F火箭的燃料是液态偏二甲肼(CH3-NH-NH-CH3),氧化剂是液态四氧化二氮。二者在反应过程中放出大量能量,同时生成无毒、无污染的气体。已知室温下,1 g燃料完全燃烧释放出的能量为42.5kJ,请写出该反应的热化学方程式________________________________________。
(1)用于发射“天宫一号”的长征二号F火箭的燃料是液态偏二甲肼(CH3-NH-NH-CH3),氧化剂是液态四氧化二氮。二者在反应过程中放出大量能量,同时生成无毒、无污染的气体。已知室温下,1 g燃料完全燃烧释放出的能量为42.5kJ,请写出该反应的热化学方程式________________________________________。
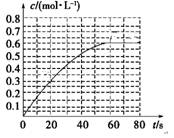
(2)298 K时,在2L的密闭容器中,发生可逆反应:2NO2(g) N2O4(g) ΔH=-a kJ·mol-1 (a>0) 。N2O4的物质的量浓度随时间变化如图。达平衡时, N2O4的浓度为NO2的2倍,回答下列问题。
N2O4(g) ΔH=-a kJ·mol-1 (a>0) 。N2O4的物质的量浓度随时间变化如图。达平衡时, N2O4的浓度为NO2的2倍,回答下列问题。
①298k时,该反应的平衡常数为________ L ·mol-1。
②下列事实能判断该反应处于平衡状态的是
a.混合气体的密度保持不变
b.混合气体的颜色不再变化
c. V(N2O4)正=2V(NO2)逆
 ③若反应在398K进行,某时刻测得n(NO2)=0.6 mol n(N2O4)=1.2mol,则此时
③若反应在398K进行,某时刻测得n(NO2)=0.6 mol n(N2O4)=1.2mol,则此时
V(正) V(逆)(填“>”“<”或“=”)。
(3)NH4HSO4在分析试剂、医药、电子工业中用途广泛。现向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。
试分析图中a、b、c、d、e五个点,
①水的电离程度最大的是__________;
②其溶液中c(OH-)的数值最接近NH3·H2O的电离常
数K数值的是 ;
③在c点,溶液中各离子浓度由大到小的排列顺序
是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某原电池总反应为:Cu+2Fe3+==Cu2++2Fe2+ 下列能实现该反应的原电池是
| A | B | C | D | |
| 电极材料 | Cu、Zn | Cu、Ag | Cu、C | Cu、Zn |
| 电解液 | FeCl3 | Fe2(SO4)3 | Fe(NO3)3 | CuSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
将等物质的量的A、B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g) XC(g)+2D(g),经5分钟后,测得D的浓度为0.5mol/L,CA:CB=3:5,C的平均速率为0.1mol/L.min。求
XC(g)+2D(g),经5分钟后,测得D的浓度为0.5mol/L,CA:CB=3:5,C的平均速率为0.1mol/L.min。求
(1)此时CA=
(2)反应开始前容器中的A、B的物质的量nA=nB=
(3)B的平均反应速率VB=
(4)X=
(5)此时容器内的压强与反应开始时压强的比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
HA为酸性略强于醋酸的一元弱酸,在0.1mol/L NaA溶液中,离子浓度关系正确的是( )
A.c(Na+) > c(A-) > c(H+) > c(OH-)
B.c(Na+) > c(A-) > c(OH-) > c(H+)
C.c(Na+) + c(OH-) = c(A-) + c(H+)
D.c(Na+) + c(H+) = c(A-) + c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:
2SO2 (g) + O2 (g)  2SO3(g) △H<0。回答下列问题:
2SO3(g) △H<0。回答下列问题:
(1)该反应450℃时平衡常数_____________500℃时平衡常数(填“大于”、“小于”或“等于”)
(2)下列描述中,能说明该反应已达到平衡的是_________________________
A.v正(O2) = 2v逆(SO3)
B.容器中气体的平均相对分子质量不随时间而变化
C.容器中气体的密度不随时间而变化
D.容器中气体的分子总数不随时间而变化
(3)在一个固定容积为5L的密闭容器中充入0.20mol SO2和0.10mol O2,半分钟后达到平衡,测得容器中含SO3 0.18mol,则v(O2) = __________________mol/(L·min),若继续通入0.20mol SO2和0.10mol O2,则平衡_____________________移动(填“向正反应方向”、“向逆反应反应”或“不”),再次达到平衡后,__________mol < n(SO3) < __________mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于甲烷性质叙述中不正确的是 ( )
A.甲烷是一种无色无味的气体 B.甲烷的密度比空气的密度小
C.甲烷极难溶解于水 D.甲烷性质稳定,不和其它物质反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各溶液中,微粒的物质的量浓度关系表述正确的是( )
A.0.1 mol·L-1 Na2CO3溶液中:c(Na+)=c(HCO )+c(H2CO3)+2c(CO
)+c(H2CO3)+2c(CO )
)
B.常温下,pH=4的醋酸与pH=10的NaOH溶液等体积混合后pH<7
C.将0.2 mol·L-1 NaA溶液和0.1 mol·L-1盐酸溶液等体积混合所得碱性溶液中:c(Na+)+c(H+)=c(A-)+c(Cl-)
D.pH=12的Ba(OH)2溶液和pH=12的Na2CO3溶液中,水电离的c(H+)相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com