
| 杂质 | 试剂 | 分离方法 | ||
| A | 乙烷 | 乙烯 | H2 | 催化转化 |
| B | 乙酸乙酯 | 乙醇 | 饱和Na2CO3溶液 | 分液 |
| C | 溴苯 | 溴 | CCl4 | 萃取 |
| D | 乙醇 | 水 | 无 | 蒸馏 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.乙烷中易引入新杂质氢气;
B.乙醇与水互溶,乙酸乙酯与碳酸钠溶液分层;
C.溴溴苯均易溶于四氯化碳;
D.乙醇与水易形成共沸混合物.
解答 解:A.乙烷中易引入新杂质氢气,不能除杂,应选溴水、洗气,故A错误;
B.乙醇与水互溶,乙酸乙酯与碳酸钠溶液分层,然后分液可分离,故B正确;
C.溴溴苯均易溶于四氯化碳,不能除杂,应选NaOH溶液、分液,故C错误;
D.乙醇与水易形成共沸混合物,不能分离,应加CaO后蒸馏,故D错误;
故选B.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、发生的反应、混合物分离方法为解答的关键,侧重分析与应用能力的考查,注意有机物性质的应用,题目难度不大.


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:选择题
| A. | 向浓氨水中滴加饱和FeCl3溶液,可以制得Fe(OH)3胶体 | |
| B. | 为除去Mg(OH)2固体中少量Ca(OH)2,可用饱和MgCl2溶液多次洗涤后,再水洗、干燥 | |
| C. | 向溶液X中加入足量盐酸,产生无色无味气体,将气体通入澄清石灰水,产生白色沉淀,说明溶液X中含有CO32- | |
| D. | 验证炭与浓硫酸反应产生的CO2,将炭与浓硫酸反应生成的气体通入盛有澄清石灰水的试管中,观察是否有白色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaA溶液的pH>7(室温下) | |
| B. | pH试纸显示0.1 mol/L HA溶液的pH为2~3(室温下) | |
| C. | 0.1 mol/L的HCl和HA溶液,前者的导电能力明显更强 | |
| D. | HA溶液能与CH3COONa溶液反应生成CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素X:它的原子中 M 层比L 层少 2 个电子 | |
| B. | 元素Y:它的焰色反应颜色呈紫色 | |
| C. | 元素Z:它的二价阳离子核外电子总数与氩原子相同 | |
| D. | 元素W:位于元素周期表中的第三周期,ⅢA 族 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol甲烷(CH4)分子中所含电子数为9NA | |
| B. | 24g镁原子的最外层电子数为NA | |
| C. | 在标准状况下,1 mol H2和1mol H2O所占的体积都约是22.4L | |
| D. | 在标准状况下,22.4L由N2和N2O组成的混合气体中,所含有的氮原子的物质的量2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
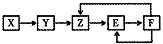 五种常见物质X、Y、Z、E、F均含有同一元素M,已知Y是单质,Z是NO(一氧化氮),在一定条件下它们有如下转化关系,下列推断不合理的是( )
五种常见物质X、Y、Z、E、F均含有同一元素M,已知Y是单质,Z是NO(一氧化氮),在一定条件下它们有如下转化关系,下列推断不合理的是( )| A. | X可能是一种氢化物 | B. | M不可能是金属 | ||
| C. | E可能是一种有色气体 | D. | X→Y一定是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
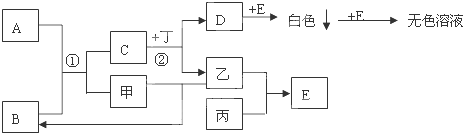
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com