
【题目】下列指定反应的离子方程式正确的是( )
A.氯气溶于水:Cl2+H2O=2H++Cl﹣+ClO﹣
B.Na2CO3溶液中CO ![]() 的水解:CO
的水解:CO ![]() +H2O=HCO
+H2O=HCO ![]() +OH﹣
+OH﹣
C.酸性溶液中KIO3与KI反应生成I2:IO3﹣+I﹣+6H+=I2+3H2O
D.NaHCO3溶液中加足量Ba(OH)2溶液:HCO ![]() +Ba2++OH﹣=BaCO3↓+H2O
+Ba2++OH﹣=BaCO3↓+H2O
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】常温下,将pH=3的盐酸和pH=11的氨水等体积混合,完全反应后,溶液中离子浓度关系正确的是( )
A.c(NH ![]() )>c(Cl﹣)>c(OH﹣)>c(H+)
)>c(Cl﹣)>c(OH﹣)>c(H+)
B.c(NH ![]() )>c(Cl﹣)>c(H+)>c(OH﹣)
)>c(Cl﹣)>c(H+)>c(OH﹣)
C.c(Cl﹣)>c(NH ![]() )>c(H+)>c(OH﹣)
)>c(H+)>c(OH﹣)
D.c(Cl﹣)>c(NH ![]() )>c(OH﹣)>c(H+)
)>c(OH﹣)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+ . 现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中正确的是( ) 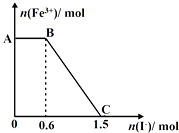
A.开始加入的K2Cr2O7为0.45mol
B.图中AB段的氧化剂为K2Cr2O7
C.图中BC段发生的反应为Fe3++2I﹣→Fe2++I2
D.K2Cr2O7可与FeSO4反应的物质的量为3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酰氯(SO2Cl2)是一种重要的化工试剂,实验室合成硫酰氯的实验装置如图所示:已知:①SO2(g)+Cl2(g)SO2Cl2(l)+Q(Q>0)
②硫酰氯常温下为无色液体,熔点为﹣54.1℃,沸点为69.1℃,在潮湿空气中“发烟”;
③100℃以上或长时间存放硫酰氯都易分解,生成二氧化硫和氯气.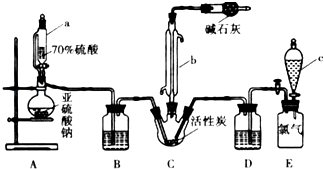
(1)仪器a为恒压分液漏斗,与普通分液漏斗相比,其优点是 .
(2)装置C中干燥管里碱石灰作用是 . 装置E为储气装置,用于提供氯气,当装置E中排出氯气1.12L(已折算成标准状况)时,最终得到5.4g纯净的硫酰氯,则硫酰氯的产率为 . 为提高硫酰氯的产率,本实验操作中还需要注意的事项有
(3)反应结束后,将C装置中三颈烧瓶里的混合物分开的实验操作是 , 氯磺酸(ClSO3H)加热分解,也能制得硫酰氯与另外一种物质,该反应的化学方程式
(4)若将SO2、Cl2按照一定比例通入水中,请设计简单实验验证二者是否恰好完全反应. .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,实验室利用如图所示装置,通过测电压求算 Ksp(AgCl).工作一段时间后,两电极质量均增大.下列说法错误的是( ) 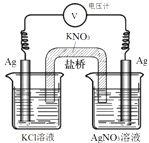
A.该装置工作时化学能转化为电能
B.左池中的银电极作正极
C.总反应为Ag+(aq)+Cl﹣(aq)AgCl(s)
D.盐桥中的K+向右池方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】11.9g金属锡(Sn)跟100mL 12molL﹣1 HNO3共热一段时间.完全反应后测定溶液中c(H+)为8molL﹣1 , 溶液体积仍为100mL.产生的气体全部被氢氧化钠溶液吸收,消耗氢氧化钠0.4mol.由此推断氧化产物可能是( )
A.SnO24H2O
B.Sn(NO3)4
C.Sn(NO3)2
D.Sn(NO3)2和Sn(NO3)4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列说法正确的是( )
A.分别中和pH相同的等体积的盐酸和醋酸溶液,消耗等量的NaOH
B.pH=a的CH3COOH溶液加水稀释10n倍后,pH=a+n
C.pH相等的CH3COONa、NaOH溶液中,水的电离程度相同
D.Na2CO3溶液中:c(OH﹣)=c(H+)+c(HCO ![]() )+2c(H2CO3)
)+2c(H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在盛有KI溶液的试管中,滴入适量氯水充分反应后,再加四氯化碳振荡,静置后观察到的现象是( )
A.上层紫红色,下层接近无色
B.均匀、透明,紫红色
C.均匀、透明,无色
D.上层接近无色,下层紫红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PbO2受热分解为Pb的+4和+2价的混合氧化物,+4价的Pb能氧化浓盐酸生成Cl2;现将1mol PbO2加热分解得到O2 , 向剩余固体中加入足量的浓盐酸得到Cl2 , O2和Cl2的物质的量之比为1:1,则剩余固体的组成及物质的量比可能是( )
A.1:2:1混合的PbO2、Pb3O4、PbO
B.1:3:2混合的PbO2、Pb3O4、PbO
C.1:1:1混合的PbO2、Pb3O4、PbO
D.2:1:1混合的PbO2、Pb3O4、PbO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com