
| A. | 升高温度,W 的体积分数减小,△H 增大 | |
| B. | 以 Y 的浓度变化表示的反应速率为 0.01 mol/(L•s) | |
| C. | 在其它条件不变的情况下,增加 1 mol X,则 X 和 Y 的转化率均提高 | |
| D. | 再向容器中通入 2 mol X 和 1 mol Y,达到平衡时,X、Y 的转化率均增大 |
分析 A.△H<0可知,反应为放热反应,则升高温度平衡逆向移动,焓变与平衡移动无关;
B.经20s达到平衡时生成了 0.4molW,结合反应可知转化的Y为0.4mol×$\frac{1}{2}$=0.2mol,结合v=$\frac{△c}{△t}$计算;
C.增加 1 mol X,促进Y的转化,但X的总量增加的多;
D.体积不变,再向容器中通入 2 mol X 和 1 mol Y,物质的量增大,压强增大,该反应为气体体积减小的反应,则平衡正向移动.
解答 解:A.反应为放热反应,则升高温度平衡逆向移动,W 的体积分数减小,但△H 不变,故A错误;
B.经20s达到平衡时生成了 0.4molW,结合反应可知转化的Y为0.4mol×$\frac{1}{2}$=0.2mol,以 Y 的浓度变化表示的反应速率为$\frac{\frac{0.2mol}{2L}}{20s}$=0.005 mol/(L•s),故B错误;
C.增加 1 mol X,促进Y的转化,但X的总量增加的多,则X的转化率减小,而Y 的转化率提高,故C错误;
D.体积不变,再向容器中通入 2 mol X 和 1 mol Y,物质的量增大,压强增大,该反应为气体体积减小的反应,则平衡正向移动,则达到平衡时,X、Y 的转化率均增大,故D正确;
故选D.
点评 本题考查化学平衡,为高频考点,把握平衡移动、速率及转化率计算为解答的关键,侧重分析与应用能力的考查,选项A为易错点,题目难度不大.


科目:高中化学 来源: 题型:解答题
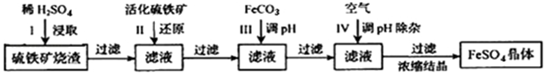
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
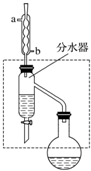 乙酸丁酯是重要的化工原料,具有水果香味.实验室制备乙酸丁酯的反应、装置示意图和有关信息如下:
乙酸丁酯是重要的化工原料,具有水果香味.实验室制备乙酸丁酯的反应、装置示意图和有关信息如下:| 乙酸 | 正丁醇 | 乙酸丁酯 | |
| 熔点/℃ | 16.6 | -89.5 | -73.5 |
| 沸点/℃ | 117.9 | 117 | 126.0 |
| 密度/g•cm-3 | 1.1 | 0.80 | 0.88 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  由如图知,石墨转变为金刚石是放热反应 | |
| B. |  由如图知,S(g)+O2(g)═SO2(g)△H1,S(s)+O2(g)═SO2(g)△H2则△H1<△H2 | |
| C. |  由如图知,白磷比红磷稳定 | |
| D. |  如由图知,CO(g)+H2O(g)═CO2(g)+H2(g)△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
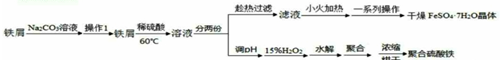
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
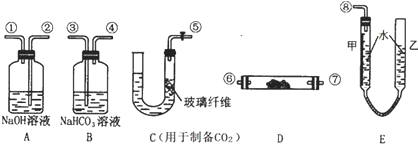
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com