
【题目】碳酸氢钠是一种重要的化工原料,在日常生活中也有广泛的用途,侯德榜先生发明了连续生产纯碱与氯化铵的联合制碱工艺,成为近代化学工业的奠基人之一,该反应原理为:![]() 饱和
饱和![]() .
.
现用如图所示装置和上述原理制取碳酸氢钠晶体,图中夹持装置已略去.
可选用的药品有:①石灰石②生石灰③![]() 盐酸④稀硫酸⑤浓氨水⑥饱和氯化钠溶液⑦饱和碳酸氢钠溶液
盐酸④稀硫酸⑤浓氨水⑥饱和氯化钠溶液⑦饱和碳酸氢钠溶液
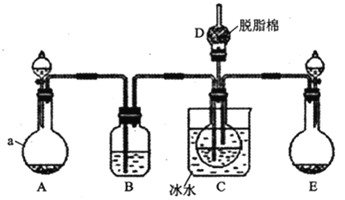
请回答下列问题
(1)仪器a的名称是______.
(2)![]() 中应选用的药品是______
中应选用的药品是______![]() 填序号
填序号![]()
(3)在实验过程中,应先向C中通入的气体的化学式是______,其原因是______.
(4)![]() 中脱脂棉应浸润的试剂是______
中脱脂棉应浸润的试剂是______![]() 填写字母编号
填写字母编号![]()
![]() 浓硫酸
浓硫酸 ![]() 稀硫酸
稀硫酸 ![]() 氢氧化钠溶液
氢氧化钠溶液 ![]() 浓硝酸
浓硝酸
(5)该小组同学为了测定C中所得晶体中碳酸氢钠的纯度![]() 假设晶体中不含碳酸盐杂质
假设晶体中不含碳酸盐杂质![]() ,先将晶体充分干燥后,称量质量为wg,称量质量为wg,然后进行如下图所示实验:
,先将晶体充分干燥后,称量质量为wg,称量质量为wg,然后进行如下图所示实验:

![]() 操作Ⅲ中的方法是______,______,______
操作Ⅲ中的方法是______,______,______
![]() 所得晶体中碳酸氢钠的纯度是______
所得晶体中碳酸氢钠的纯度是______![]() 不必化简
不必化简![]()
【答案】圆底烧瓶 ⑦ ![]()
![]() 在水中溶解度小,先通
在水中溶解度小,先通![]() 至饱和,有利于
至饱和,有利于![]() 析出 b 过滤 洗涤 干燥
析出 b 过滤 洗涤 干燥 ![]()
【解析】
![]() 根据常用的仪器名称解答;
根据常用的仪器名称解答;
![]() 装置的作用为除去二氧化碳中的氯化氢,二氧化碳在饱和碳酸氢钠溶液中溶解度不大,氯化氢能够与碳酸氢钠反应生成二氧化碳;
装置的作用为除去二氧化碳中的氯化氢,二氧化碳在饱和碳酸氢钠溶液中溶解度不大,氯化氢能够与碳酸氢钠反应生成二氧化碳;
![]() 根据二氧化碳和氨气的溶解性判断先通入的气体,氨气极易溶于水,易于二氧化碳的吸收,所以应先通入氨气;
根据二氧化碳和氨气的溶解性判断先通入的气体,氨气极易溶于水,易于二氧化碳的吸收,所以应先通入氨气;
![]() 氨气易挥发,氨气为碱性气体,与酸反应、与碱不反应,浓硫酸具有强氧化性,浓硝酸易挥发;
氨气易挥发,氨气为碱性气体,与酸反应、与碱不反应,浓硫酸具有强氧化性,浓硝酸易挥发;
![]() 测定C中所得晶体的碳酸氢钠的纯度
测定C中所得晶体的碳酸氢钠的纯度![]() 假设晶体中不含碳酸盐杂质
假设晶体中不含碳酸盐杂质![]() ,将晶体充分干燥后,称量质量为wg,此时为碳酸氢钠粗品质量,操作1将晶体加热到质量不再变化时,所得粉末为碳酸钠和杂质,然后溶解,加入氢氧化钡溶液,氢氧化钡跟碳酸钠反应生成碳酸钡,将生成的碳酸钡过滤、洗涤、干燥,称量为ng,根据关系式
,将晶体充分干燥后,称量质量为wg,此时为碳酸氢钠粗品质量,操作1将晶体加热到质量不再变化时,所得粉末为碳酸钠和杂质,然后溶解,加入氢氧化钡溶液,氢氧化钡跟碳酸钠反应生成碳酸钡,将生成的碳酸钡过滤、洗涤、干燥,称量为ng,根据关系式![]() --
--![]() 可求出纯碳酸氢钠的质量。
可求出纯碳酸氢钠的质量。
![]() 装置为制取二氧化碳的装置,仪器a为圆底烧瓶,故答案为:圆底烧瓶;
装置为制取二氧化碳的装置,仪器a为圆底烧瓶,故答案为:圆底烧瓶;
![]() 装置的作用为除去二氧化碳中的氯化氢,二氧化碳在饱和碳酸氢钠溶液中溶解度不大,氯化氢能够与碳酸氢钠反应生成二氧化碳,所以B中盛有试剂为饱和碳酸氢钠溶液,
装置的作用为除去二氧化碳中的氯化氢,二氧化碳在饱和碳酸氢钠溶液中溶解度不大,氯化氢能够与碳酸氢钠反应生成二氧化碳,所以B中盛有试剂为饱和碳酸氢钠溶液,
故答案为:![]() ;
;
![]() 在水中溶解度小,氨气极易溶于水,则先通
在水中溶解度小,氨气极易溶于水,则先通![]() 至饱和,然后通入二氧化碳气体,有利于
至饱和,然后通入二氧化碳气体,有利于![]() 析出,
析出,
故答案为:![]() ;
;![]() 在水中溶解度小,先通
在水中溶解度小,先通![]() 至饱和,有利于
至饱和,有利于![]() 析出;
析出;
![]() 氨气易挥发,D中脱脂棉应浸润的试剂吸收逸出的氨气,浓硫酸能使棉花脱水、浓硝酸具有挥发性,氨气为碱性气体,与硫酸反应,所以选择稀硫酸,
氨气易挥发,D中脱脂棉应浸润的试剂吸收逸出的氨气,浓硫酸能使棉花脱水、浓硝酸具有挥发性,氨气为碱性气体,与硫酸反应,所以选择稀硫酸,
故答案为:b;
![]() 测定C中所得晶体的碳酸氢钠的纯度
测定C中所得晶体的碳酸氢钠的纯度![]() 假设晶体中不含碳酸盐杂质
假设晶体中不含碳酸盐杂质![]() ,将晶体充分干燥后,称量质量为wg,此时为碳酸氢钠粗品质量,操作1将晶体加热到质量不再变化时,所得粉末为碳酸钠和杂质,然后溶解,加入氢氧化钡溶液,氢氧化钡跟碳酸钠反应生成碳酸钡,将生成的碳酸钡过滤、洗涤、干燥,称量为
,将晶体充分干燥后,称量质量为wg,此时为碳酸氢钠粗品质量,操作1将晶体加热到质量不再变化时,所得粉末为碳酸钠和杂质,然后溶解,加入氢氧化钡溶液,氢氧化钡跟碳酸钠反应生成碳酸钡,将生成的碳酸钡过滤、洗涤、干燥,称量为![]() ,
,
反应的化学方程式为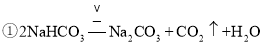 ,
,![]() ,得到的碳酸钡需要经过过滤、洗涤、干燥后方可称量.
,得到的碳酸钡需要经过过滤、洗涤、干燥后方可称量.
设样品中碳酸氢钠的质量为x,由上两式可得关系式:

![]() ,
,![]() ,
,
所得晶体中碳酸氢钠的纯度![]() 。
。


科目:高中化学 来源: 题型:
【题目】下列关于![]() 的说法正确的是
的说法正确的是
A. 所有原子可能都在同一平面上 B. 最多只可能有9个碳原子在同一平面
C. 有7个碳原子可能在同一直线 D. 只可能有5个碳原子在同一直线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组研究铝土矿中Al2O3的含量.查阅资料得知,铝土矿的主要成分是Al2O3,杂质是Fe2O3、SiO2等。从铝土矿中提取Al2O3的过程如下:

(1)提取前将铝土矿“粉碎”目的是__________。
(2)固体B的主要用途有________________(写出一条即可)。
(3)第①步,向铝土矿中加入足量烧碱溶液,充分反应,发生反应的离子方程式有: _____________(至少写一个)。
(4)第②步中加入过量盐酸的目的是____________________;实验室配制200mL 8mol/L的盐酸需要的玻璃仪器有__________________。
(5)能否把第③步中的氨水换成氢氧化钠__________,理由___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用吸附了氢气的纳米碳管等材料制作的二次电池的原理如图所示。下列说法正确的是( )
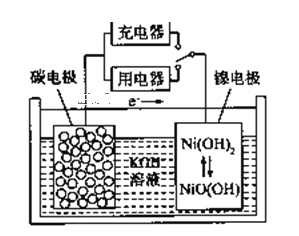
A. 充电时,阴极的电极反应为:Ni(OH)2+OH-+e-=NiO(OH)+H2O
B. 放电时,负极的电极反应为:H2-2e-+2OH-=2H2O
C. 放电时,OH-移向镍电极
D. 充电时,将电池的碳电极与外电源的正极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式为 ,分析其结构,并回答下列问题:
,分析其结构,并回答下列问题:
(1)写出其分子式:____________________________________________。
(2)其中含有____个不饱和碳原子,分子中有____个双键。
(3)分子中的极性键有__________(写出2种即可)。
(4)分子中的饱和碳原子有______个,一定与苯环处于同一平面的碳原子有______个。
(5)分子中C—C===O键角约为__________,H—C≡C键角约为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是元素周期表的草图,表中所列字母代号分别代表某一种元素,请回答:

(1)表中最活泼的金属与最活泼的非金属形成的物质是__________________(填化学式)。
(2)由a、d两种元素可形成两种化合物,写出其中一种化合物分解生成另一种化合物的化学方程式:_____________________,
(3)e、f、k、m对应的单原子离子的半径由大到小的顺序为__________(填离子符号)。
(4)d、m对应的离子还原性由强到弱顺序为_________________________(填离子符号)。
(5)d、e、m的气态氢化物中,最不稳定的是________________________(填分子式)。
(6)用电子式表示n与m形成的原子个数比2∶1的化合物的形成过程:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知非金属单质硫(S)是淡黄色固体粉末,难溶于水。为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:

(1)装置A的分液漏斗中盛装的试剂是______,烧瓶中加入的试剂是______。
(2)画出虚线框内的实验装置图____________,并注明所加试剂,说明装置的作用_____________。
(3)装置B中盛放的试剂是_____(选填下列所给试剂的代码),实验现象为________,化学反应方程式是________________。
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
(4)从原子结构的角度简要分析氯元素的非金属性比硫元素的非金属性强的原因。_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. PH=1的醋酸加水稀释到原体积的100倍,稀释后PH=3
B. 室温 pH=3的醋酸溶液和pH=11的Ba(OH)2溶液等体积混合后溶液呈酸性
C. 室温pH相同的NH4Cl溶液和CH3COOH溶液,由水电离产生的c(H+)相同
D. 某温度下,水的离子积常数为1×10-12,该温度下PH=7的溶液呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语表达不正确的是( )
①丙烷的球棍模型 ②丙烯的结构简式为CH3CHCH2
②丙烯的结构简式为CH3CHCH2
③某有机物的名称是2,3-二甲基戊烷 ④![]() 与C8H6互为同分异构体
与C8H6互为同分异构体
A. ①②B. ②③C. ②④D. ③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com