
| A. | 12gNaH中阴离子所含电子总数为NA | |
| B. | 60gSiO2含有的化学键数目为4NA | |
| C. | CO2通过Na2O2使其增重ag时,反应中转移的电子数为$\frac{a{N}_{A}}{56}$ | |
| D. | 常温常压下,14.9gKCl与NaClO的固体混合物中阴离子的数目为0.2NA |
分析 A、求出NaH的物质的量,然后根据NaH中含12个电子来分析;
B、求出二氧化硅的物质的量,然后根据1mol二氧化硅中含4mol硅氧键来分析;
C、1mol二氧化碳和过氧化钠反应时,反应增重28g,转移1mol电子;
D、KCl与NaClO的摩尔质量均为74.5g/mol,且均由一个阴离子和一个阳离子构成.
解答 解:A、12gNaH的物质的量为0.5mol,而NaH中含12个电子,故0.5molNaH中含6NA个电子,故A错误;
B、60g二氧化硅的物质的量为1mol,而1mol二氧化硅中含4mol硅氧键,故含4NA条,故B正确;
C、1mol二氧化碳和过氧化钠反应方程式为:2Na2O2+2CO2=2Na2CO3+O2,反应增重28g,转移1mol电子,故当增重ag时,转移的电子的物质的量n=$\frac{a}{28}$mol,个数为$\frac{a}{28}{N}_{A}$个,故C错误;
D、KCl与NaClO的摩尔质量均为74.5g/mol,故14.9g混合物的物质的量为0.2mol,且两者均由一个阴离子和一个阳离子构成,故0.2mol混合物中含0.2NA个阴离子,故D正确.
故选AC.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 禁止使用含铅汽油,原因是铅资源短缺 | |
| B. | 增长汽车排气管的长度可以降低尾气中CO和NO的含量 | |
| C. | 目前国内销售的加碘食盐中,碘以KIO3的形式存在 | |
| D. | 光化学烟雾是大量排放SO2引起的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4+2O2$\stackrel{点燃}{→}$ CO2+2H2O | B. | 2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O | ||
| C. | CH4$\stackrel{高温}{→}$ C+2H2 | D. | 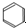 +HO-NO2$→_{△}^{浓硫酸}$H2O+ +HO-NO2$→_{△}^{浓硫酸}$H2O+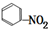 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 装有尾气净化装置的汽车排出的气体中不再含有NO或CO | |
| B. | 升温能使反应物活化分子的百分数增加,所以提高尾气净化效率还需要升高温度 | |
| C. | 提高尾气净化效率的最佳途径是研制高效催化剂 | |
| D. | 因该反应正向进行的程度已经很大,故使用催化剂并无实际意义 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
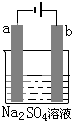 图为直流电源电解1L 0.2mol/L的CuSO4水溶液的装置.通电一段时间后,b电极共收集到4.48L的气体(标准状况下),然后在石墨电极a和b附近分别滴加一滴石蕊试液,下列关于实验的叙述中不正确的是( )
图为直流电源电解1L 0.2mol/L的CuSO4水溶液的装置.通电一段时间后,b电极共收集到4.48L的气体(标准状况下),然后在石墨电极a和b附近分别滴加一滴石蕊试液,下列关于实验的叙述中不正确的是( )| A. | a电极的产物有Cu和H2 | |
| B. | 反应一段时间后,溶液的pH值变小 | |
| C. | a电极附近呈红色,b电极附近出现蓝色. | |
| D. | a、b电极转移的电子数为0.4mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有甲酸乙酯和甲酸 | B. | 有甲酸乙酯和乙醇 | ||
| C. | 有甲酸乙酯,可能有乙醇 | D. | 几种物质都有 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 长期使用(NH4)2SO4化肥会使土壤酸化,而过度使用尿素[CO(NH2)2]会使土壤碱化 | |
| B. | 锅炉水垢中含有的CaSO4,可先用Na2CO3溶液处理,后用酸除去 | |
| C. | 利用CO2合成聚碳酸酯类可降解塑料,实现“碳”的循环利用 | |
| D. | 神舟10号飞船所用太阳能电池板可将光能转换为电能,所用转换材料是SiO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 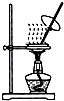 蒸发FeCl3溶液得氯化铁晶体 | |
| B. | 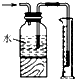 测量氯气的体积 | |
| C. |  作为制取少量SO2的尾气吸收装置 | |
| D. | 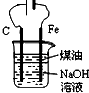 制备Fe(OH)2并能较长时间观察其颜色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 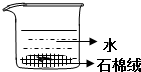 | B. | 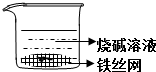 | ||
| C. | 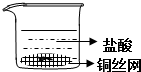 | D. | 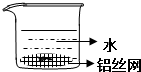 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com