
常见的五种盐A、B、C、D、E,它们的阳离子可能是Na+、NH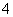 、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、NO
、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、NO 、SO
、SO 、CO
、CO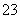 ,已知:
,已知:
①五种盐均溶于水,水溶液均为无色。
②D的焰色反应呈黄色。
③A的溶液呈中性,B、C、E的溶液呈酸性,D的溶液呈碱性。
④若在这五种盐的溶液中分别加入Ba(NO3)2溶液,只有A、C的溶液不产生沉淀。
⑤若在这五种盐的溶液中,分别加入氨水,E和C的溶液中生成沉淀,继续加氨水,C中沉淀消失。
⑥把A的溶液分别加入到B、C、E的溶液中,均能生成不溶于稀硝酸的沉淀。
请回答下列问题:
(1)五种盐中,一定没有的阳离子是____________;所含阴离子相同的两种盐的化学式是__________________。
(2)D的化学式为__________________,D溶液显碱性的原因是________________________________________________________________________(用离子方程式表示)。
(3)A和C的溶液反应的离子方程式是________________________________________________________________________;
E和氨水反应的离子方程式是________________________________________________________________________。
(4)若要检验B中所含的阳离子,正确的实验方法是________________________________________________________________________
________________________________________________________________________。
答案 (1)Cu2+、Fe3+ (NH4)2SO4、Al2(SO4)3
(2)Na2CO3 CO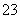 +H2O??HCO
+H2O??HCO +OH-
+OH-
(3)Ag++Cl-===AgCl↓ Al3++3NH3·H2O===Al(OH)3↓+3NH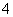
(4)取少量B于试管中,加入浓NaOH溶液并加热,用湿润的红色石蕊试纸放在试管口,观察是否变蓝色
解析 由于盐溶液没有颜色,所以没有Cu2+和Fe3+;根据实验现象可知,A、B、C、D、E分别为BaCl2、(NH4)2SO4、AgNO3、Na2CO3、Al2(SO4)3;检验NH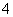 ,常用的方法是将铵盐与浓NaOH溶液共热,看是否能够产生使湿润的红色石蕊试纸变蓝的气体。
,常用的方法是将铵盐与浓NaOH溶液共热,看是否能够产生使湿润的红色石蕊试纸变蓝的气体。


科目:高中化学 来源: 题型:
将足量的SO2通入下列各溶液中,所含离子还能大量共存的是( )
A.K+、SiO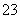 、Cl-、NO
、Cl-、NO
B.H+、NH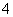 、Al3+、SO
、Al3+、SO
C.Na+、Cl-、MnO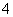 、SO
、SO
D.Na+、CO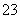 、CH3COO-、HCO
、CH3COO-、HCO
查看答案和解析>>
科目:高中化学 来源: 题型:
某未知溶液可能含Cl-、CO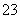 、Na+、SO
、Na+、SO 、Al3+,将溶液滴在蓝色石蕊试纸上,试纸变红。取少量试液,滴加硝酸酸化的氯化钡溶液,有白色沉淀生成;在上层清液中滴加硝酸银溶液,产生白色沉淀。下列判断合理的是( )
、Al3+,将溶液滴在蓝色石蕊试纸上,试纸变红。取少量试液,滴加硝酸酸化的氯化钡溶液,有白色沉淀生成;在上层清液中滴加硝酸银溶液,产生白色沉淀。下列判断合理的是( )
A.一定有Cl- B.一定有SO
C.一定没有Al3+ D.可能有CO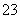
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.遇苯酚变紫色的溶液:Na+、Mg2+、SO 、Cl-
、Cl-
B.0.1 mol·L-1(NH4)2Fe(SO4)2溶液中:K+、Cu2+、Cl-、MnO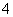
C.使甲基橙变红色的溶液:NH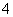 、Cu2+、ClO-、Cl-
、Cu2+、ClO-、Cl-
D. 0.1 mol·L-1 NaHCO3溶液:K+、AlO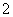 、Cl-、NO
、Cl-、NO
查看答案和解析>>
科目:高中化学 来源: 题型:
依据Mg、Al单质的性质,思考回答下列问题。
(1)铝的化学性质活泼,为什么日常生活中广泛使用的铝制品通常具有较好的抗腐蚀性能?
(2)Al既能溶于强酸,又能溶于强碱,所以说“Al既有金属性,又有非金属性”你认为这种说法是否恰当?为什么?
(3)铝与酸、碱反应的实质是什么?氧化剂是什么?
(4)镁在空气中充分燃烧,所得固体产物可能有哪些:________________(用化学式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
烟气脱硫能有效减少二氧化硫的排放。实验室用粉煤灰(主要含Al2O3、SiO2等)制备碱式硫酸铝[Al2(SO4)x(OH)6-2x]溶液,并用于烟气脱硫研究。
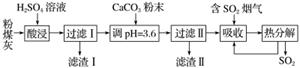
(1)酸浸时反应的化学方程式为________________________________;滤渣Ⅰ的主要成分为________________(填化学式)。
(2)加CaCO3调节溶液的pH至3.6,其目的是中和溶液中的酸,并使Al2(SO4)3转化为Al2(SO4)x(OH)6-2x。滤渣Ⅱ的主要成分为________________________(填化学式);若溶液的pH偏高,将会导致溶液中铝元素的含量降低,其原因是________________________________________(用离子方程式表示)。
(3)上述流程中经完全热分解放出的SO2量总是小于吸收的SO2量,其主要原因是________________________________;与吸收SO2前的溶液相比,热分解后循环利用的溶液的pH将________(填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
2008年的秋天,毒奶粉事件震动全国,这主要是奶粉中含有有毒的三聚氰胺(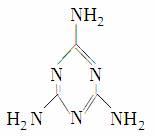 )。下列关于三聚氰胺分子的说法中正确的是( )
)。下列关于三聚氰胺分子的说法中正确的是( )
A.所有氮原子均采取sp3杂化
B.一个三聚氰胺分子中共含有15个σ键
C.属于极性分子,故极易溶于水
D.三聚氰胺分子中只含有极性键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com