
���������л����ϩ���Ҵ������ᡢ��������������
��1����ֱ�д�����к������¹����ŵ��л�������ƣ�
�ٴ��ǻ�_________���ڡ�COOH____________��
��2�������������л����У���д��ţ�
�ټ��ܷ����ӳɷ�Ӧ�����ܷ����ۺϷ�Ӧ����_____________��
���ܷ���ˮ�ⷴӦ����_______________��
��3���ѱ����뵽ʢ����ˮ���Թ��У�Һ�����ֲַ�����������ã����ֳȺ�ɫҺ���һ����__________����ϡ����¡�����
��4���ѱ����뵽ʢ���������Ը��������Һ���Թ��У������Ը��������Һ����ɫ��˵����������_________����С���û�С���̼̼˫����

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016������и�����ѧ�ڵ�����¿����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ʶ�Ӧ����;����ȷ���ǣ�
A | B | C | D | |
���� | Һ�� | ̼��� | �Ȼ��� | Ũ���� |
��; | ����� | ����ҩ | ������ | ��ʴ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�갲��ʡ��һ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ȥ���������������Լ��ͷ�������ȷ���ǣ� ��
A��Cu��Fe�����������������ᣬ���� B��KNO3��NaCl�������ؽᾧ
C��ˮ��NaCl���������� D��CO2��HCl����������������Һ��ϴ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ�ʡ�߶��϶������Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʵ�������ȫ��ȷ����
A������к͵ζ�������ʵ�飺���Ժͼ�¼pH�ļ��ʱ��Ҫ��ͬ
B������һ��Ũ�ȵ��Ȼ�����Һ0.1mol/L��ȷ��ȡ�Ȼ��ع��壬��Ͳ��ȡ1000mlˮ��������ƿ�У��ܽ⣬��ҡ�ȣ�����
C���ų���ʽ�ζ��ܼ��첿�ֵ����ݣ�����������ʹ������������ϣ�����ָ��ס���ܣ����ἷѹ�����飬ʹ��Һ�Ӽ�������
D��ȡ����Һ©����������ϲ�Һ�壺�²�Һ��ӷ�Һ©���¶˼�ڷų����رջ�������һ�������������ϲ�Һ������ӷ�Һ©���¶˹ܿڷų�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭��ʡ�߶������У�������ѧ�Ծ��������棩 ���ͣ������
��ش��������⣺
��1���л���M����̫������տ�ת��ΪN��ת���������£�

��M��N��ȣ����ȶ����� _________
��2��25�������£�pH=4��������Һ����ˮ���������H+��Ũ��Ϊ_______mol/L
��3����֪CH3OH��ȼ���ȡ�H= -akJ•mol-1��CH3OH(l)+1/2O2(g)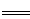 CO2(g)+2H2(g)��H= -bkJ•mol-1����a_____b���>������<����=������
CO2(g)+2H2(g)��H= -bkJ•mol-1����a_____b���>������<����=������
��4��ʹCl2��H2O(g)ͨ�����ȵ�̿�㣬����HCl��CO2������1molCl2���뷴Ӧʱ�ͷų�145kJ������д���÷�Ӧ���Ȼ�ѧ����ʽ��_____________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭��ʡ�߶������У��ģ���ѧ�Ծ��������棩 ���ͣ�ѡ����
�������������뻯ѧʽ�������ȷ����
A�������ơ�NaNO2 B����������-FeO C������-�� D���ƾ�-ȩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���㽭ʡ������ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
�ϳɰ��������ѧ�����ϵ�һ���ش�ͻ�ƣ��䷴Ӧԭ��Ϊ��
N2(g)+3H2(g) 2NH3(g) ∆H= ��92.4kJ•mol?1 һ�ֹ�ҵ�ϳɰ��ļ�������ͼ���£�
2NH3(g) ∆H= ��92.4kJ•mol?1 һ�ֹ�ҵ�ϳɰ��ļ�������ͼ���£�
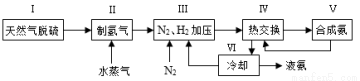
��1����Ȼ���е�H2S���ʳ��ð�ˮ���գ�д����ˮ�ĵ��뷽��ʽ �����ղ���ΪNH4HS��һ����������NH4HS��Һ��ͨ��������õ�������ʹ����Һ������д������Һ������Ӧ�Ļ�ѧ����ʽ ��
��2������II��������ԭ�����£�
��CH4(g)+H2O(g)  CO(g)+3H2(g) ��H=+206.4 kJ��mol-1
CO(g)+3H2(g) ��H=+206.4 kJ��mol-1
��CO(g)+ H2O(g)  CO2(g)+H2(g) ��H=��41.2 kJ��mol-1
CO2(g)+H2(g) ��H=��41.2 kJ��mol-1
��ӦCH4(g)+2H2O(g)  CO2(g)+4H2(g) ��H= kJ��mol-1��
CO2(g)+4H2(g) ��H= kJ��mol-1��
���ڷ�Ӧ�٣�һ���������ƽ����ϵ��H2�ٷֺ��������ܼӿ췴Ӧ���ʵĴ�ʩ�ǣ����ţ� ��
a�������¶� b������ˮ����Ũ�� c��������� d������ѹǿ
��3�����÷�Ӧ�ڣ���CO��һ��ת���������H2��������1mol CO��H2�Ļ�����壨CO���������Ϊ20%����H2O������Ӧ���õ�1.18mol CO��CO2��H2�Ļ�����壬��COת����Ϊ ��
��4����ͼ1��ʾ500�桢60.0MPa�����£�H2��N2Ϊԭ������Ͷ�ϱ���ƽ��ʱNH3��������Ĺ�ϵ���� ��ͼ��a�����ݼ���N2��ƽ���������Ϊ ��
��5�������¶ȶԺϳɰ���Ӧ��Ӱ�죬����ͼ2����ϵ�У�����һ�������µ��ܱ������ڣ���ͨ����ʼԭ������ʼ�����¶Ȳ������ߣ�NH3���ʵ����仯������ʾ��ͼ��
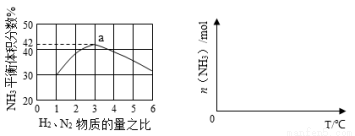
ͼ1 ͼ2
��6����������������ߺϳɰ�ԭ����ת���ʵķ��� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�������и߶������в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���ܱ������У�һ�������½������·�Ӧ2NO(g)+2CO(g) N2(g)+2CO2(g)����H����373.2kJ��mol-1���ﵽƽ���Ϊ��߸÷�Ӧ�����ʺ�NO��ת���ʣ���ȡ����ȷ��ʩ�ǣ� ��
N2(g)+2CO2(g)����H����373.2kJ��mol-1���ﵽƽ���Ϊ��߸÷�Ӧ�����ʺ�NO��ת���ʣ���ȡ����ȷ��ʩ�ǣ� ��
A���Ӵ���ͬʱ�����¶� B���Ӵ���ͬʱ����ѹǿ
C�������¶�ͬʱ����N2 D�������¶�ͬʱ����ѹǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�츣��ʡ������ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ij��ҵ��ˮ�����±��е�ijЩ���ӣ��Ҹ������ӵ����ʵ���Ũ����ȣ���Ϊ0.1mol/L������ֵ����ˮ�ĵ��뼰���ӵ�ˮ�⣩��
������ | K+ Ag+ Mg2+ Cu2+ Al3+ NH4+ |
������ | Cl- CO32- NO3- SO42- I- |
��ͬѧ��̽����ˮ����ɣ�����������ʵ�飺
��ȡ����ɫ��Һ5mL���μ�һ�ΰ�ˮ�г������ɣ��������������ӡ�
���ò�˿պȡ��Һ���ڻ��������գ�����ɫ�ܲ����۲죬����ɫ���档
����ȡ��Һ����������ᣬ����ɫ�������ɣ�����ɫ������������ɺ���ɫ��
������������õ���Һ�м���BaCl2��Һ���а�ɫ�������ɡ������ƶϲ���ȷ���ǣ�
A���ɢ��жϣ���Һ��һ�������е���������K+��NH4+��Cu2+
B�����м�������������ɫ��������ӷ���ʽ��6I-+2NO3-+8H+�T3I2+2NO��+4H2O
C��ԭ��Һһ��ֻ���е�����I-��NO3-��SO42-��Mg2+��Al3+
D����ȡ100mLԭ��Һ������������NaOH��Һ����ַ�Ӧ����ˣ�ϴ�ӣ����ճ��������أ��õ��Ĺ�������Ϊ0.4g
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com