
【题目】SO2气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下两个化学反应:
①SO2+2Fe3++2H2O=SO42-+2Fe2++4H+;
②Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O。
下列有关说法错误的是
A. 氧化性:Cr2O72->Fe3+>SO2
B. K2Cr2O7能将Na2SO3氧化成Na2SO4
C. 每有1 mol K2Cr2O7参加反应,转移电子的数目为6NA
D. 若有6.72 L SO2(标准状况)参加反应,则最终消耗0.2 mol K2Cr2O7
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案科目:高中化学 来源: 题型:
【题目】下列各组离子能在无色酸性溶液中大量共存的是( )
A. Ba2+、Mg2+、Cl﹣、NO3﹣ B. Na+、Ca2+、CO32﹣、NO3﹣
C. Cu2+、K+、SO42﹣、NO3﹣ D. Na+、HCO3﹣、OH﹣、Ca2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝分别与足量的稀盐酸和氢氧化钠溶液反应时,当两个反应放出的气体在相同状况下体积相等时,反应中消耗的盐酸和氢氧化钠的物质的量之比为( )
A. 1∶1 B. 2∶1 C. 3∶1 D. 1∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用石油产品A(C3H6)为主要原料,合成具有广泛用途的有机玻璃PMMA。流程如下(部分产物和条件省略)

试回答下列问题:
(1)B的名称________;X试剂为_______(化学式);D中官能团名称_________。
(2)E→G的化学方程式为________________________________________,反应类型是_________。
(3)T是G的同分异构体,1molT与足量新制Cu(OH)2悬浊液反应最多生成2molCu2O沉淀,T的结构有________种(不含立体结构)。
(4)若高分子化合物PMMA的相对分子质量为1.5×106,其聚合度为_______。
(5)参照上述流程,以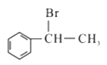 为原料合成
为原料合成 (其它原料自选)。设计合成路线:________________________。
(其它原料自选)。设计合成路线:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.用苯可以萃取溴水中的溴单质
B.蒸馏时,应将温度计水银球插入液面下
C.为了使过滤速率加快,可用玻璃棒在过滤器中轻轻搅拌,加速液体流动
D.凡是给玻璃仪器加热,都要垫石棉网,以防仪器炸裂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定某有机含氧化合物A的结构,通过实验得出以下数据: ①将有机化合物A置于氧气流中充分燃烧,实验测得生成5.4g H2O和8.8g CO2 .
②利用质谱仪测定出有机化合物A的相对分子质量为46.
③该有机物可与金属钠反应,生成氢气.
请回答:
(1)有机化合物A中碳原子与氢原子的个数比是 , A的结构简式为 .
(2)化合物A在一定条件下脱水可生成B,B可加聚合成包装塑料.A转化为B的化学反应方程式为 .
(3)化合物A可在一定条件下通过粮食制得,由粮食制得的A在一定温度下密闭储存,由于发生一系列的化学变化而变得有酯香味.在这一系列变化过程中,最后一步化学变化的化学方程式为 , 反应类型为 .
(4)体育比赛中当运动员肌肉扭伤时,队医随即用氯乙烷(沸点为12.27oC)对受伤部位进行局部冷冻麻醉.请用B选择合适的方法制备氯乙烷,要求原子利用率为100%,制备反应方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。
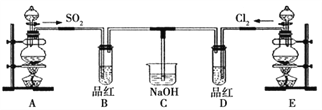
(1)实验室用装置A制备SO2。从物质类别看,SO2属于________(填“酸性”、“两性”或“碱性”)氧化物;
(2)实验室用装置E制备Cl2,写出该反应的离子方程式:___________________________。当有0.2 mol电子转移时,产生氯气的体积(标准状况)是________,氧化剂与还原剂的物质的量之比是________。
(3)反应开始一段时间后,观察到B、D两个试管中的品红溶液均褪色。停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为B:________________,D:________________。
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强,他们将制得的SO2和Cl2按1︰1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示)____________________________。
(5)有人预测SO2能使酸性高锰酸钾溶液褪色,你认为该预测是否合理?________(填“合理”或“不合理”),理由是________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com