
【题目】铬铁矿的主要成分可以表示为FeOCr2O3 , 还含有SiO2、Al2O3杂质,以铬铁矿为原料制备重铬酸钾(K2Cr2O7)过程如图所示. 
已知:CrO42﹣和Cr2O72﹣在酸性条件下可以相互转化.
请回答下列问题:
(1)完成并配平下列方程式: 6FeO+6Cr2O3+KOH+KClO3=K2CrO4+Fe2O3+KCl+
(2)滤渣1的成分是(填化学式),滤液1的成分除K2CrO4、KClO3、KOH外,还含有(填化学式),过滤后洗涤沉淀的操作是 .
(3)试剂1是(填化学式),利用滤渣2可制得两种氧化物,其中一种氧化物经电解冶炼可获得金属,电解时阴极的电极反应式为 .
(4)对滤液2用稀硫酸酸化处理时发生的离子反应方程式是 , 酸化处理时往往增大稀硫酸浓度的原因是 .
(5)检验氯酸钾晶体中钾元素的具体方法是 .
【答案】
(1)24;7;12;3;7;12H2O
(2)Fe2O3;KAlO2、K2SiO3;沿玻璃棒注入蒸馏水至浸没沉淀,等蒸馏水自然流下,重复以上操作2﹣3次
(3)HCl;Al3++3e﹣=Al
(4)2CrO42﹣+2H+?Cr2O72﹣+H2O;增大反应物浓度,平衡正向移动,有利于提高产物的产率
(5)用洁净的铂丝蘸取待测液,放到酒精灯外焰灼烧,透过蓝色的钴玻璃,观察到紫色火焰证明钾元素存在
【解析】解:(1)根据质量守恒,方程为:6FeO+6Cr2O3+24KOH+7KClO3=12K2CrO4+3Fe2O3+7KCl+12H2O;所以答案是:24;7;12;3;7;12H2O;(2)由分析可知,将铬铁矿和氯酸钾、氢氧化钾高温熔融,得到K2CrO4、K2SiO3、KAlO2、Fe2O3 , 然后水浸,过滤得到滤渣1和滤液1,滤渣1为Fe2O3 , 滤液1中主要是K2CrO4、KClO3、KOH、KAlO2、K2SiO3;过滤后沿玻璃棒注入蒸馏水至浸没沉淀,等蒸馏水自然流下,重复以上操作2﹣3次洗涤沉淀;
所以答案是:Fe2O3;KAlO2、K2SiO3;沿玻璃棒注入蒸馏水至浸没沉淀,等蒸馏水自然流下,重复以上操作2﹣3次;(3)试剂1为酸,可选盐酸,利用滤渣2可得到氧化铝、二氧化硅,电解得金属则电解氧化铝,阴极反应为:Al3++3e﹣=Al;
所以答案是:HCl;Al3++3e﹣=Al;(4)对滤液2用稀硫酸酸化处理时发生的离子反应方程式是:2CrO42﹣+2H+Cr2O72﹣+H2O;增大稀硫酸浓度的原因是增大反应物浓度,平衡正向移动,有利于提高产物的产率;
所以答案是:2CrO42﹣+2H+Cr2O72﹣+H2O;增大反应物浓度,平衡正向移动,有利于提高产物的产率;(5)检验钾元素可用焰色反应,方法为:用洁净的铂丝蘸取待测液,放到酒精灯外焰灼烧,透过蓝色的钴玻璃,观察到紫色火焰证明钾元素存在;
所以答案是:用洁净的铂丝蘸取待测液,放到酒精灯外焰灼烧,透过蓝色的钴玻璃,观察到紫色火焰证明钾元素存在.


 每课必练系列答案
每课必练系列答案科目:高中化学 来源: 题型:
【题目】一定温度下向体积为2L的恒容密闭容器中充入6molCO2和8mo1H2 , 发生反应:CO2 (g)+3H2(g)=CH3OH(g)+H2O(g)△H=﹣49KJmol﹣1 . 测得n(H2)物质的量随时间变化如曲线I 所示,下列说法正确的是( ) 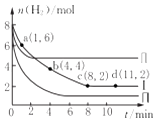
A.该反应在O~8min内的v(CO2)=0.125molL﹣1min﹣1
B.若起始时向容器中充入3mo1CO2和4molH2 , 则平衡时CH3OH的体积分数大于20%
C.若起始时向容器中充入4mo1CO2和2molH2、2molCH3OH、1molH2O(g),则此时反应v(正)>v(逆)
D.曲线II、曲线III改变条件分别是升高温度、减小压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于1.5mol 氢气的叙述中,正确的是( )
A. 质量是 4g
B. 体积是 33.6L
C. 电子数是 3
D. 分子数约为1.5×6.02×1023个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋中有丰富的食品、矿产、能源、药物和水产等资源,如图表示海水综合利用的部分过程.下列说法不正确的是( ) 
A.工业上通过电解熔融状态MgCl2制取金属镁
B.用澄清石灰水可鉴别NaHCO3和Na2CO3
C.在第②、④步骤中,溴元素均被氧化
D.制取NaHCO3的反应中,利用了其溶解度在相同条件下小于NaCl的性质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物J是在医疗上有重要的应用,分子结构中含有3个六元环.其中一种合成路线如图: 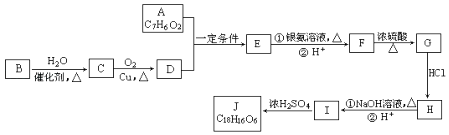
已知:
①A既能发生银镜反应,又能与FeCl3溶液发生显色反应,其核磁共振氢谱显示有4个吸收峰,且峰面积之比为1:2:2:1.
②有机物B是一种重要的石油化工产品,其产量可用来衡量国家的石油化工发展水平.
③R1﹣CHO+R2﹣CH2﹣CHO ![]()
![]()
请回答下列问题:
(1)E的结构简式是 , G中含氧官能团的名称 .
(2)写出有机反应类型H→I , F→G .
(3)写出I生成J的化学方程式 .
(4)A的含苯环同分异构体有种,写出其中符合以下要求的同分异构体的结构简式 . ①能发生银镜反应 ②能发生水解反应 ③含有苯环
(5)写出用B合成 ![]() 的路线图(提示:路线图的书写方法RCH=CH2
的路线图(提示:路线图的书写方法RCH=CH2![]()
![]()
![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.1mol/L的H2C2O4溶液中H2C2O4、HC2O4﹣、C2O42﹣三者中所占物质的量分数〔分布系数)随pH变化的关系如图所示.下列表述不正确的是( ) 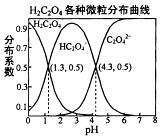
A.HC2O4﹣H++C2O42﹣ , K=1×10﹣4.3
B.将等物质的量的NaHC2O4、NAa2C2O4溶于水中,所得溶液PH恰好为4.3
C.常温下HF的KB=1×10﹣﹣3.45 , 将少量H2C2O4溶液加入到足量NaF溶液中,发生的反应为:H2C2O4+F﹣=HF+HC2O4﹣
D.在0.1mol/LNaHC2O4溶液中,各离子浓度大小关系为:c(Na+)>c(HC2O4﹣)>c(C2O42﹣)>c(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列应用或事实与胶体的性质没有关系的是
A. 用明矾净化饮用水
B. 用石膏或盐卤点制豆腐
C. 在FeCl3溶液中滴加NaOH溶液出现红褐色沉淀
D. 清晨的阳光穿过茂密的林木枝叶所产生的美丽景象(美丽的光线)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 蛋白质都是由C、H、N、O四种元素组成的
B. 天然蛋白质水解的最终产物均为α氨基酸
C. 强酸、强碱和重金属盐都可使蛋白质变性
D. 构成蛋白质的某些氨基酸人体自身是不能合成的
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com